题目内容
8.小强同学用三支试管,分别取适量的稀盐酸、澄清石灰水、碳酸钠溶液,进行相关实验探究.步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性;步骤2:小强把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色;
步骤3:把烧杯中的混合物进行过滤,得到滤液,滤液中一定不含有A.
(选填答案:A.稀盐酸 B.澄清石灰水 C.碳酸钠溶液 )
【实验猜想】步骤3所得滤液中溶质可能为:
①NaCl Na2CO3; ②NaCl CaCl2和NaOH;③NaCl Na2CO3和NaOH④…..
【实验验证】(提示CaCl2溶液显中性)
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 有白色沉淀产生且红色不消失 | 猜想③成立 |
分析 显碱性的溶液能使酚酞试液变红色;
显酸性的溶液不能使酚酞试液变色;
氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠;
稀盐酸能和碳酸钠反应生成氯化钠、水和二氧化碳,能和氢氧化钠反应生成氯化钠和水.
解答 解:步骤1:向三支试管中分别滴加酚酞后,Na2CO3溶液中显红色,说明,Na2CO3溶液显碱性.
故填:碱.
步骤3:因为把三支试管中的溶液同时倒入一只烧杯中,发现有气泡产生,最终有白色沉淀生成且溶液显红色,说明溶液显碱性,因此滤液中一定不含有稀盐酸.
故填:A.
【实验验证】实验过程如下表所示:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 有白色沉淀产生且红色不消失 | 猜想③成立 |
故填:若改为稀盐酸,只能证明碳酸钠的存在,无法证明氢氧化钠的存在.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
19.下列括号中是除去少量杂质所用的方法或试剂,其中错误的是( )
| A. | CaO中的CaCO3(高温煅烧) | B. | CO2中的CO(点燃) | ||
| C. | CO中的CO2(澄清的石灰水) | D. | N2中的O2(灼热铜丝) |
3.下列化学方程式能正确表示所述内容的是( )
| A. | 酸雨的形成:CO2+H2O=H2CO3 | |
| B. | 中和反应:H2SO4+MgO=MgSO4+H2O | |
| C. | Fe和盐酸反应:2Fe+6HCl=2FeCl3+3H2↑ | |
| D. | 研究水的组成:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
13.下列现象中属于物理变化的是( )
| A. | 钢铁生锈 | B. | 煤的燃烧 | C. | 冰融化成水 | D. | 火药爆炸 |
18.MP2.5中文名为“细微颗粒物”,细颗粒物只是地球大气成分中含量很少的组分,但它对空气质量和能见度等有重要的影响.下列不属于细微颗粒物来源的是( )
| A. | 绿色植物的花粉 | B. | 火山爆发出的火山灰 | ||
| C. | 光合作用产生的氧气 | D. | 森林大火产生的灰尘 |
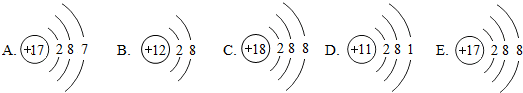
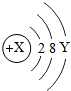 为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.
为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.