题目内容
11.二氧化碳和氢氧化钠可发生如下的化学反应:CO2+2NaOH═Na2CO3+H2O.求:(1)NaOH的相对分子质量是:40.
(2)CO2中碳元素与氧元素的质量比为:3:8.
(3)2.2g CO2与NaOH反应,最多可制得Na2CO3多少g?
分析 根据化学方程式计算的步骤有:一设、二写、三找、四列、五答、六查.在本题中,NaOH的相对分子质量=23+16+1=40;CO2中碳元素与氧元素的质量比=12:(16×2)=3:8;有关化学方程式的计算要准确.
解答 解:(1)在本题中,NaOH的相对分子质量=23+16+1=40;故答案为:40
(2)CO2中碳元素与氧元素的质量比=12:(16×2)=3:8;故答案为:3:8
(3)解:设最多可制得Na2CO3的质量为x.
CO2+2NaOH=Na2CO3+H2O
44 106
2.2g x
$\frac{44}{106}=\frac{2.2g}{x}$ x=5.3g
答:最多可制得Na2CO3的质量为5.3g.
故答案为:5.3g;
点评 本考点考查了根据化学方程式的计算,属于质量分数和化学方程式的综合应用,是中考计算题中经常出现的题型.做题时要注意:化学方程式要写正确,有关化学式的相对分子质量计算要正确,始终不要忘记质量守恒定律,本考点主要出现在计算题中.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
1.在ZnO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Zn+CO2的反应中,氧化剂是( )
| A. | CO | B. | Zn | C. | ZnO | D. | CO2 |
2.许多人喜欢染发,经调查染发剂中常含有对苯二胺(化学式为C6H8N2)它有致癌作用,建议不要染发,下列有关对苯二胺分析正确的是( )
| A. | 由三种元素组成 | |
| B. | 氢元素所占质量分数最小 | |
| C. | 属于有机物 | |
| D. | 碳、氢、氮三种元素的质量比为3:4:1 |
19.下列括号中是除去少量杂质所用的方法或试剂,其中错误的是( )
| A. | CaO中的CaCO3(高温煅烧) | B. | CO2中的CO(点燃) | ||
| C. | CO中的CO2(澄清的石灰水) | D. | N2中的O2(灼热铜丝) |
3.下列化学方程式能正确表示所述内容的是( )
| A. | 酸雨的形成:CO2+H2O=H2CO3 | |
| B. | 中和反应:H2SO4+MgO=MgSO4+H2O | |
| C. | Fe和盐酸反应:2Fe+6HCl=2FeCl3+3H2↑ | |
| D. | 研究水的组成:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ |
1.甲、乙、丙三位同学对氯化镁样品(仅含氯化钠杂质)进行如下检测:各取10g样品溶于一定量的水中得到50g溶液,再分别加入质量不同,溶质质量分数均为10%的氢氧化钠溶液,反应得到沉淀的实验数据如表:
试回答下列问题:
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
| 甲 | 乙 | 丙 | |
| 加入氢氧化钠溶液质量 (g) | 70 | 80 | 90 |
| 反应得到沉淀的质量 (g) | 5 | 5.8 | 5.8 |
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
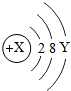 为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.
为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.