题目内容
14.化学学科的特征是在原子、分子水平上研究物质.请从微观角度回答下列问题:(1)物质的结构决定物质性质.一氧化碳和二氧化碳化学性质不同的原因是:分子构成不同
(2)微粒的运动和性质决定了宏观物质的变化.化学变化遵循质量守恒定律是因为反应前后①④⑤不变.(从下列选项中选择,填序号)
①原子种类 ②分子种类 ③分子数目 ④原子的质量 ⑤原子数目
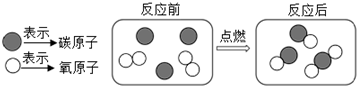
(3)如图是煤燃烧过程中某反应的微观示意图,反应前,有两 种单质;生成物是混合物(填“化合物”“混合物”);为了使煤充分燃烧达到节能减排之目的,在反应物中应增加的微粒是氧分子填微粒名称).
(4)物质丙是重要的化工产品,在国民经济中占有重要地位.工业上用甲和乙合成丙.甲、乙、丙的微观示意图如表.
| 物 质 | 甲 | 乙 | 丙 |  -氮原子 -氮原子 -氢原子 -氢原子 |
示意图 | 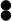 | 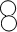 |  |
②甲、乙、丙中属于化合物的是丙(填序号) ③写出物质丙的化学式NH3
④甲和乙合成丙的反应中,甲、乙、丙的微粒个数之比为3:1:2
⑤根据物质的微观示意图学出甲和乙在高温、高压、催化剂的条件下反应生成丙的化学方程式为3H2+N2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
分析 (1)根据二氧化碳是由二氧化碳分子构成,而一氧化碳是由一氧化碳分子构成进行解答;
(2)根据质量守恒定律的内涵来分析;
(3)根据微观示意图体现的意义进行解答;
(4)根据微观反应示意图来分析.
解答 解:(1)二氧化碳是由二氧化碳分子构成,而一氧化碳是由一氧化碳分子构成,所以一氧化碳和二氧化碳的化学性质不同,是由于构成它们的分子不同,故填:分子构成不同;
(2)在化学反应前后,原子的种类、数目、质量均不发生改变;分子的种类一定改变、分子的数目可能改变;故填:①④⑤;
(3)由图示可知,反应一种由同种原子构成的物质,属于单质,另一种是由同种分子构成的,而该分子是由同种原子构成的,也属于单质;而生成物是两种物质,属于混合物,在氧气充足的条件下,碳完全燃烧生成二氧化碳,由微观示意图可知,应为氧气分子,故填:两;混合物;氧分子;
(4)①由图可知,甲、乙、丙三种物质都是由分子构成的;故填:分子;
②化合物是由多种元素组成的,微观上是由多种原子构成的,故甲、乙、丙中属于化合物的是丙;故填:丙;
③每个丙的分子是由1个氮原子和3个氢原子构成的,故填:NH3
④氢气和氮气反应生成氨气,该反应的化学方程式为3H2+N2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,甲、乙、丙的微粒个数比为 3:1:2.故填:3:1:2;
⑤氢气和氮气反应生成氨气,该反应的化学方程式为3H2+N2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3,故填:3H2+N2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
点评 根据变化微观示意图及粒子构成模拟图,根据分子由原子构成等特点,正确判断变化中的物质构成,是解答本题的基本方法.

 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案| A. | 蔗糖是由碳、氢、氧原子构成的 | B. | 蔗糖属于有机物 | ||
| C. | 蔗糖中碳、氧元素的质量比为12:11 | D. | 蔗糖中氢元素的质量分数最大 |
| A. | 浓硫酸沾到皮肤上,立即用大量水冲洗 | |
| B. | 酒精在桌面燃起来用嘴吹灭 | |
| C. | 用肥皂水区分蒸馏水和硝酸镁溶液 | |
| D. | 进入久未开肩的菜窖前,应先做灯火实验 |
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | S+O2$\frac{\underline{\;燃烧\;}}{\;}$SO2↑ | ||
| C. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | D. | 2P+5O2$\frac{\underline{\;点燃\;}}{\;}$P2O3 |

 水在生活、生产和化学实验中起着十分重要的作用.
水在生活、生产和化学实验中起着十分重要的作用.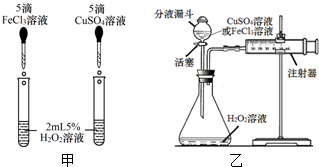 教材指出:H2O2分解的催化剂并非只有二氧化锰一种.实验证明FeCl3溶液、CuSO4溶液、红砖粉末都可以代替二氧化锰作H2O2分解的催化剂.针对上述结论,南开中学初三化学兴趣小组进行了如下探究:
教材指出:H2O2分解的催化剂并非只有二氧化锰一种.实验证明FeCl3溶液、CuSO4溶液、红砖粉末都可以代替二氧化锰作H2O2分解的催化剂.针对上述结论,南开中学初三化学兴趣小组进行了如下探究: