题目内容
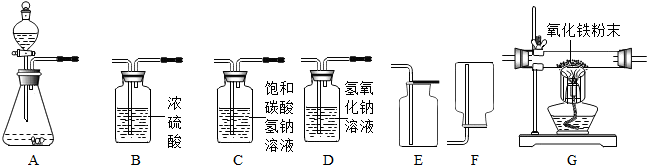
6.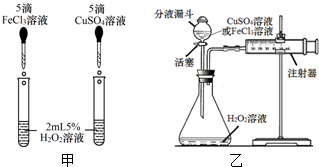 教材指出:H2O2分解的催化剂并非只有二氧化锰一种.实验证明FeCl3溶液、CuSO4溶液、红砖粉末都可以代替二氧化锰作H2O2分解的催化剂.针对上述结论,南开中学初三化学兴趣小组进行了如下探究:
教材指出:H2O2分解的催化剂并非只有二氧化锰一种.实验证明FeCl3溶液、CuSO4溶液、红砖粉末都可以代替二氧化锰作H2O2分解的催化剂.针对上述结论,南开中学初三化学兴趣小组进行了如下探究:探究一:
比较同浓度FeCl3溶液、CuSO4溶液的催化效果
(1)请写出甲图左侧试管H2O2分解的化学方程式:2H2O2$\frac{\underline{\;FeCl_{3}溶液\;}}{\;}$2H2O+O2↑.
(2)如用图甲装置进行实验,应观察同时滴入两种溶液后产生气泡的快慢的现象.
(3)如用图乙装置进行实验,实验前检查该装置气密性良好.应测量生成等体积气体时所需的时间.
(4)已知过氧化氢分解是一个放热反应.用图乙装置进行实验时,细心的小丽同学观察到,锥形瓶中不再产生气泡后注射器的活塞向左移了一小段,请你推测出现该现象的原因温度降低,装置内压强减小.
探究二:证明红砖粉末可以作过氧化氢分解的催化剂
(5)小熊同学设计了如下实验:
她分别取2mL5%的H2O2溶液于两试管中,再称取0.5g红砖粉末倒入其中一支试管,发现加了红砖粉末的一支试管产生气泡速率较快.小熊认为,由此可证明红砖粉末可以作过氧化氢分解的催化剂.
小陈同学认为小熊的证明过程不够严密,需要补充下面两项实验.
实验结束后,小陈将试管内的剩余药品经①过滤、洗涤、干煤后,称量得到固体质量仍为0.5g.
应补充的另一项实验为(填写实验操作)②将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率.
分析 (1)根据反应的原理来分析;
(2)根据产生气体的速率来分析;
(3)根据比较催化效果的方法来分析;
(4)根据温度变化来分析;
(5)从液体中分离出固体的方法是过滤;结合催化剂的特征来分析.
解答 解:(1)过氧化氢在氯化铁溶液的催化作用下分解为水和氧气,故填:2H2O2$\frac{\underline{\;FeCl_{3}溶液\;}}{\;}$2H2O+O2↑;
(2)用图甲装置进行实验,应观察同时滴入两种溶液后产生气泡的快慢来判断催化效果,故填:产生气泡的快慢;
(3)催化剂的催化效果越好,反应产生气体的速率越快,可通过测量产生等体积的氧气所需要的时间来分析,所需时间越短,催化效果越好;故填:时间;
(4)由于该反应是个放热反应,反应完全结束后,温度降低,注射器以及装置内的压强变小,在外界大气压的作用下,活塞向内移动一点;故填:温度降低,装置内压强减小;
(5)从反应后的液体中分离出难溶性的红砖粉采用过滤的方法;要证明它是否属于催化剂,不但要看是否改变了反应速率、质量是否改变,还需要看其化学性质是否改变.
故答案为:过滤;将过滤、洗涤、干燥后的红砖粉放入一只盛有过氧化氢溶液的试管中,观察产生气泡的速率.
点评 本题考查实验装置的综合应用,为高频考点,把握反应速率测定原理及影响反应速率的因素为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
16.长期饮用硬水对人体健康不利,一些工业用水也不能使用硬水.下列方法能够用来区别硬水和软水的是( )
| A. | 观察颜色 | B. | 加入明矾 | C. | 通入氧气 | D. | 加入肥皂水 |
17.以下说法中不正确的是( )
| A. | 离子是带电粒子,但带电的粒子不一定是离子 | |
| B. | 氧化物中含有氧元素,但含氧元素的化合物不一定是氧化物 | |
| C. | 酸中都含有氢元素,只要含有氢元素的化合物都是酸 | |
| D. | 中和反应一定是复分解反应 |
14.化学学科的特征是在原子、分子水平上研究物质.请从微观角度回答下列问题:
(1)物质的结构决定物质性质.一氧化碳和二氧化碳化学性质不同的原因是:分子构成不同
(2)微粒的运动和性质决定了宏观物质的变化.化学变化遵循质量守恒定律是因为反应前后①④⑤不变.(从下列选项中选择,填序号)
①原子种类 ②分子种类 ③分子数目 ④原子的质量 ⑤原子数目
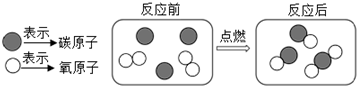
(3)如图是煤燃烧过程中某反应的微观示意图,反应前,有两 种单质;生成物是混合物(填“化合物”“混合物”);为了使煤充分燃烧达到节能减排之目的,在反应物中应增加的微粒是氧分子填微粒名称).
(4)物质丙是重要的化工产品,在国民经济中占有重要地位.工业上用甲和乙合成丙.甲、乙、丙的微观示意图如表.
①甲、乙、丙三种物质都是由分子构成(填“分子”“原子”或“离子”)
②甲、乙、丙中属于化合物的是丙(填序号) ③写出物质丙的化学式NH3
④甲和乙合成丙的反应中,甲、乙、丙的微粒个数之比为3:1:2
⑤根据物质的微观示意图学出甲和乙在高温、高压、催化剂的条件下反应生成丙的化学方程式为3H2+N2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
(1)物质的结构决定物质性质.一氧化碳和二氧化碳化学性质不同的原因是:分子构成不同
(2)微粒的运动和性质决定了宏观物质的变化.化学变化遵循质量守恒定律是因为反应前后①④⑤不变.(从下列选项中选择,填序号)
①原子种类 ②分子种类 ③分子数目 ④原子的质量 ⑤原子数目
(3)如图是煤燃烧过程中某反应的微观示意图,反应前,有两 种单质;生成物是混合物(填“化合物”“混合物”);为了使煤充分燃烧达到节能减排之目的,在反应物中应增加的微粒是氧分子填微粒名称).

(4)物质丙是重要的化工产品,在国民经济中占有重要地位.工业上用甲和乙合成丙.甲、乙、丙的微观示意图如表.
| 物 质 | 甲 | 乙 | 丙 |  -氮原子 -氮原子 -氢原子 -氢原子 |
示意图 | 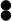 |  |  |
②甲、乙、丙中属于化合物的是丙(填序号) ③写出物质丙的化学式NH3
④甲和乙合成丙的反应中,甲、乙、丙的微粒个数之比为3:1:2
⑤根据物质的微观示意图学出甲和乙在高温、高压、催化剂的条件下反应生成丙的化学方程式为3H2+N2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
11.氯气是一种有毒的气体,实验室制取氯气时,可用氢氧化钠溶液来吸收尾气,其反应原理为Cl2+2NaOH═X+NaClO+H2O,则X 的化学式为( )
| A. | NaCl | B. | H2 | C. | HCl | D. | HClO |
18.用盐酸可以清除铁锈(主要成分为Fe2O3),盐酸中主要含有H2O分子、H+、C1-.某探究小组为探究稀盐酸中的哪种微粒能使氧化铁溶解,设计了如下实验方案,得出了初步结论.
(1)请填写下表中的实验结论:
(2)是否需要做“向Fe2O3中加入水”的对比实验否(填“是”或“否”).
(1)请填写下表中的实验结论:
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有少量Fe2O3的试管中加入NaCl溶液振荡 | 固体不溶解 | a:H2O分子不能使Fe2O3溶解 b:Cl-不能使Fe2O3溶解 |
15.下列各组生活现象中,前者属于物理变化,后者属于化学变化的一组是( )
| A. | 蜡烛燃烧,葡萄酒化 | B. | 汽车爆胎、铁器生锈 | ||
| C. | 水果腐烂、蔗糖溶解 | D. | 玻璃破碎、鲜肉冷冻 |