题目内容
9. 某中学化学学习小组的同学正在对水的电解实验进行探究
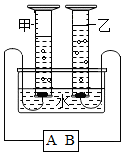
某中学化学学习小组的同学正在对水的电解实验进行探究(1)江洋同学记录的实验现象如图所示,请根据现象判断B为电源的正极.
(2)徐凡同学将水换成食盐水(主要成分为NaCl)进行电解,连接电极的两个试管都收集到气体.其中负极收集到的是无色可燃性气体,则该气体是H2(填化学式).点燃该气体前要进行的操作是验纯.
(3)徐琛同学发现连接正极的试管收集到了一种黄绿色气体.根据反应物的成分,你认为这种气体有可能是Cl2(填化学式).查阅资料后,徐琛同学了解到这种气体是由于在电解时食盐和水反应生成的,同时生成的还有氢氧化钠和负极产生的气体,请你写出该反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
分析 (1)根据电解水实验的现象、结论及生成气体的性质分析.
(2)根据气体的性质,结合质量守恒推测气体物质;
(3)根据以上分析,归纳出食盐水电解发生反应的化学方程式.
解答 解:(1)由电解水的装置可知,接通直流电源后,乙试管产生的气体较少是氧气,连接的是电源的正极;甲试管产生的气体较多是氢气,连接电源的负极.
(2)电解食盐水,反应前的物质食盐和水中共有Na、Cl、H、O四种元素,因此电解出的可燃性气体为氢气;点燃该气体前要进行的操作是验纯;
(3)徐琛同学发现连接正极的试管收集到了一种黄绿色气体.根据反应物的成分,你认为这种气体有可能是氯气;根据质量守恒定律,反应物应为氯化钠和水,化学方程式为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
答案:
(1)正;
(2)H2; 验纯
(3)Cl2;2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
点评 本题难度不大,掌握电解水的实验现象、结论(正氧负氢,氢二氧一)、生成气体的性质等即可正确解答本题.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.实验室制取二氧化碳和高锰酸钾制取氧气作比较,下列说法正确的是( )
| A. | 气体发生装置不相同 | B. | 气体收集方法不可能相同 | ||
| C. | 反应条件相同 | D. | 反应的基本反应类型相同 |
20.闻集草莓是阜阳市特色水果,阜阳市特产之一.下列操作过程中是化学变化的是( )
| A. | 采摘草莓 | B. | 清洗草莓 | ||
| C. | 用榨汁机将草莓制成果汁 | D. | 草莓酿酒 |
17.完成实验探究时,仪器的选择、使用和洗涤至关重要,下列叙述合理的是( )
| A. | 已经洗净的仪器,内壁上有许多分散比较均匀的水滴 | |
| B. | 广口瓶、滴瓶、集气瓶都有作磨砂处理 | |
| C. | 用量筒量取液体的过程中,必须始终保持量筒竖直放置于水平桌面 | |
| D. | 用托盘天平称量固体物质,物质和砝码放反了位置,测不出其质量 |
4.下列性质与用途关系错误的是( )
| A. | 活性炭具有吸附性--用于净水 | |
| B. | 氢气可燃--用作气体燃料 | |
| C. | 稀有气体的化学性质稳定--用作保护气 | |
| D. | 氧气的密度比空气略大--用于急救病人 |
14.如表是我们生活中常见的食物的近似pH:
如下的说法正确的是( )
| 物质 | 柠檬 | 鸡蛋清 | 苹果 | 西红柿 | 牛奶 |
| pH | 2.3 | 7.9 | 3.1 | 4.2 | 6.5 |
| A. | 牛奶和鸡蛋清均呈弱碱性 | B. | 胃酸过多的人应少食苹果 | ||
| C. | 柠檬汁能使酚酞试液变红 | D. | 西红柿的酸性比苹果强 |
19.贝壳的主要成分是碳酸钙,为了测定贝壳中碳酸钙的含量,现将150g稀盐酸分5次加入到25g贝壳样品中(杂质不溶于水也不参与反应),充分反应后测得生成气体的总质量见表,请计算:
(1)m的值为6.6
(2)25g贝壳样品中碳酸钙的质量.(写出计算过程)
| 1 | 2 | 3 | 4 | 5 | |
| 加入稀盐酸的质量/g | 30 | 30 | 30 | 30 | 30 |
| 生成气体的总质量/g | 2.2 | 4.4 | m | 8.8 | 8.8 |
(2)25g贝壳样品中碳酸钙的质量.(写出计算过程)
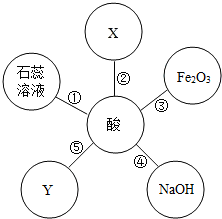 硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如图体现了酸类物质的通性,其中X、Y及图中所给其他物质的类别不同.请结合该图回答下列问题:
硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如图体现了酸类物质的通性,其中X、Y及图中所给其他物质的类别不同.请结合该图回答下列问题: