题目内容
1.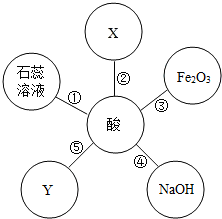 硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如图体现了酸类物质的通性,其中X、Y及图中所给其他物质的类别不同.请结合该图回答下列问题:
硫酸和盐酸是实验室常用的试剂,也是重要的化工原料,它们既有相似之处,又有不同之点.如图体现了酸类物质的通性,其中X、Y及图中所给其他物质的类别不同.请结合该图回答下列问题:(1)图中①处反应的现象是石蕊溶液变红;
(2)已知X只含有一种元素,则X可能是锌(填化学式);
(3)若此酸为稀硫酸,反应③的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)若此酸为稀盐酸,测得反应④得到的溶液pH>7,则其中的溶质为NaOH、NaCl(填化学式);
(5)若此酸为醋酸(CH3COOH),其在水溶液中电离得到CH3COO (醋酸根离子)和H+(填写离子符号),请写出一符合条件的反应⑤的化学方程式Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑.
分析 根据已有的酸的性质进行分析解答即可,酸能与指示剂、活泼金属、金属氧化物、碱以及盐发生反应,据此解答.
解答 解:(1)酸能使石蕊试液变化红,故填:石蕊溶液变红;
(2)氢前的金属能与酸反应,故可以是金属锌,故填:锌;
(3)稀硫酸能与氧化铁反应生成硫酸铁和水,故填:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(4)氢氧化钠和盐酸反应生成氯化钠和水,溶液的pH大于7,说明呈碱性,含有氢氧化钠,故填:NaOH、NaCl;
(5)醋酸(CH3COOH),其在水溶液中电离得到CH3COO (醋酸根离子)和H+;Y是盐,碳酸钠与醋酸反应生成醋酸钠、水和二氧化碳,化学方程式为:Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑.故填:H+;Na2CO3+2CH3COOH=2CH3COONa+H2O+CO2↑.
点评 本题考查的是常见的酸的性质,完成此题,可以依据已有的酸的通性进行.

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
12.水是我们最熟悉的物质之一,下列有关水的常识认识正确的是( )
| A. | 经常烧硬水的水壶,水垢较少 | |
| B. | 加热煮沸既可以消毒杀菌还可以降低水的硬度 | |
| C. | 硬水洗衣服在使用等量洗涤剂的前提下,洗涤效果更好 | |
| D. | 软水加入肥皂水,泡沫少、浮渣多 |
16.某溶液中大量存在的离子仅有Mg2+、Ca2+和X离子,则X可能是( )
| A. | Na+ | B. | OH- | C. | Cl- | D. | CO32- |
6.下列说法正确的是( )
| A. | KMnO4和K2MnO4中含有相同的原子团 | |
| B. | 质子数相同的微粒属于同一种元素 | |
| C. | 氯气(Cl2)中氯元素化合价为-1价 | |
| D. | 同一化合物中同种元素也可以显示不同的化合价 |
13.当前我国环保部正在着力推进以防治PM2.5为重点的大气污染防治工作.下列措施对PM2.5的治理不能起到积极作用的是( )
| A. | 大力植树造林 | B. | 大力发展煤炭发电 | ||
| C. | 用氢能源代替化石燃料 | D. | 禁止焚烧秸秆和垃圾 |
10. 甲、乙两种固体的溶解度曲线如右图所示,下列说法错误的是 ( )
甲、乙两种固体的溶解度曲线如右图所示,下列说法错误的是 ( )
 甲、乙两种固体的溶解度曲线如右图所示,下列说法错误的是 ( )
甲、乙两种固体的溶解度曲线如右图所示,下列说法错误的是 ( )| A. | 20℃时,甲的溶解度小于乙的溶解度 | |
| B. | 20℃时,100 g水中加入20 g甲可得到饱和溶液 | |
| C. | 20℃时,可配制溶质质量分数为30%的乙溶液. | |
| D. | 若要将组成在M点的乙溶液转变为N点的乙溶液,可升温至50℃,整个过程溶质的质量分数不变 |
 某中学化学学习小组的同学正在对水的电解实验进行探究
某中学化学学习小组的同学正在对水的电解实验进行探究 某同学用如图所示的装置和药品,制取并收集氧气.请回答:
某同学用如图所示的装置和药品,制取并收集氧气.请回答: