题目内容
8.某混合气体由C2H2、C2H4、CH4中的两种或三种气体组成,取该气体在氧气中充分燃烧,测得生成的水和二氧化碳的质量比为9:22.(1)甲烷充分燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(2)该混合气体成分的可能情况有哪几种?
分析 根据甲烷燃烧生成了二氧化碳和水,分析写出反应的方程式;
根据二氧化碳和水的质量比为22:9,可计算出碳、氢两种元素的质量比,据此解答.
解答 解:(1)甲烷燃烧生成了二氧化碳和水,反应的方程式是:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
故答案为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(2)生成的二氧化碳和水的质量比为22:9,则碳元素和氢元素的质量比为:(22×$\frac{12}{44}$):(9×$\frac{2}{18}$)=6:1,故碳氢原子的个数比为:$\frac{6}{12}:\frac{1}{1}$=1:2,
若只含有C2H4,碳氢原子的个数比为1:2;若是含一个,则能达到碳氢原子个数比是1:2,该气体可能同时含有CH4、C2H2、C2H4,能达到碳氢原子个数比是1:2,由于某混合气体由C2H2、C2H4、CH4中的两种或三种气体组成,
故答案:CH4和C2H2两种气体或C2H2、C2H4、CH4三种气体.
点评 主要考查了相对分子质量的计算和分子的构成.根据化学式进行有关的推断时,要结合质量守恒定律以及化学式的有关计算进行.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
18.下列实验设计错误的是( )
| A. | 用肥皂水可区分硬水和软水 | |
| B. | 蒸发食盐水时,出现多量固体时停止加热 | |
| C. | 用浓硫酸干燥氨气 | |
| D. | 用燃烧的方法可区分羊毛制品和棉制品 |
16. 如图是探究木炭还原氧化铜的实验装置.某同学做了该实验并记录了有关测量数据如表:(空气中的二氧化碳忽略不计)
如图是探究木炭还原氧化铜的实验装置.某同学做了该实验并记录了有关测量数据如表:(空气中的二氧化碳忽略不计)
请回答:
(1)实验时,酒精灯网罩的作用集中火焰,提高温度.
(2)本次实验结果显示:△m1>△m2.对产生上述结果的原因,有同学提出下列分析,其中合理的是ABC.
A.装置漏气
B.生成的CO2部分与过量的C反应生成了CO
C.氢氧化钠溶液的浓度太低
(3)假设产生的二氧化碳气体能被氢氧化钠溶液全部吸收,根据以上数据分析,得出产生的气体是CO、CO2,此过程中生成的Cu的质量是6.4克.
 如图是探究木炭还原氧化铜的实验装置.某同学做了该实验并记录了有关测量数据如表:(空气中的二氧化碳忽略不计)
如图是探究木炭还原氧化铜的实验装置.某同学做了该实验并记录了有关测量数据如表:(空气中的二氧化碳忽略不计)| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | 69.8g | 67.3g | △m1 |
| 烧杯+氢氧化钠溶液 | 118.8g | 119.9g | △m2 |
(1)实验时,酒精灯网罩的作用集中火焰,提高温度.
(2)本次实验结果显示:△m1>△m2.对产生上述结果的原因,有同学提出下列分析,其中合理的是ABC.
A.装置漏气
B.生成的CO2部分与过量的C反应生成了CO
C.氢氧化钠溶液的浓度太低
(3)假设产生的二氧化碳气体能被氢氧化钠溶液全部吸收,根据以上数据分析,得出产生的气体是CO、CO2,此过程中生成的Cu的质量是6.4克.
20.下列各组物质对应归类正确的是( )
| A. | 金刚石、石墨、C60--碳单质 | B. | 煤、石油、氢气一化石燃料 | ||
| C. | 氧气、水、二氧化碳--氧化物 | D. | 橡胶、羊毛、塑料--有机合成材料 |


 ,化学反应中该原子易得到(填“得到”或“失去”)电子,形成离子的符号是Cl-.
,化学反应中该原子易得到(填“得到”或“失去”)电子,形成离子的符号是Cl-.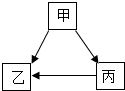 无机物甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去.
无机物甲、乙、丙经一步反应的转化关系如图所示,其中部分反应物、生成物及反应条件已略去.