题目内容
13.硝酸亚铁是一种重要的食品和饲料添加剂,某补血剂样品[主要成分为碳酸亚铁晶体(FeSO4•7H20)],某化学兴趣小组对其产生了兴趣并进行了探究:[查阅资料]
①硫酸亚铁晶体加热时,先失去结晶水:FeSO4•7H20$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4+7H2O↑
高温会继续分解,分解方程式:2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO2↑+SO3↑
②无水硫酸铜粉末遇水会变成蓝色的硫酸铜晶体;
③二氧化硫能使紫色高锰酸钾溶液褪色.
[进行实验]该兴趣小组同学称取27.8g硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行分析,并利用SDTQ600热分解仪,对硫酸亚铁晶体热分解获得相关数据,绘制成图2所示的关系图,试回答:
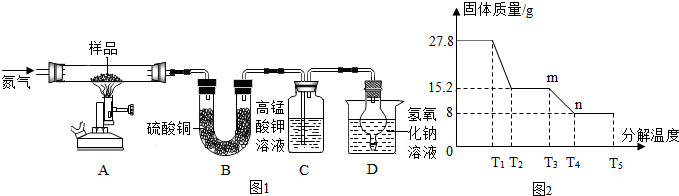
(1)硫酸亚铁晶体完全分解后,装置A中的固体变为红棕色的Fe2O3,装置B中硫酸铜粉末变蓝,说明产物中有水;装置C中的现象紫色的高锰酸钾溶液褪色.
(2)根据图2中的数据,计算生成二氧化硫的质量是多少.
分析 (1)根据无水硫酸铜白色粉末遇水变蓝,所以常用来检验水的存在,二氧化硫能使高锰酸钾溶液褪色,所以常用来检验二氧化硫的存在进行分析;
(2)根据硫酸亚铁晶体加热时,先失去结晶水,高温会继续分解生成氧化铁、二氧化硫和三氧化硫,结合图象中的数据进行计算.
解答 解:(1)无水硫酸铜白色粉末遇水变蓝,所以常用来检验水的存在,二氧化硫能使高锰酸钾溶液褪色,所以常用来检验二氧化硫的存在,所以硫酸亚铁晶体完全分解后,装置A中的固体变为红棕色的Fe2O3,装置B中硫酸铜粉末变蓝,说明产物中有水,装置C中的现象是紫色的高锰酸钾溶液褪色;
(2)通过图象中的数据可以看出,第一次固体质量减少是硫酸亚铁晶体分数分解,第二次固体质量减少是硫酸亚铁分数分解,所以
设生成二氧化硫的质量为x
2FeSO4$\frac{\underline{\;高温\;}}{\;}$Fe2O3+SO3↑+SO2↑
304 160 64
15.2g 8g x
$\frac{160}{8g}$=$\frac{64}{x}$
x=3.2g
故答案为:(1)水,紫色的高锰酸钾溶液褪色;
(2)生成二氧化硫的质量是3.2g.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列各组粒子中,核外电子数不相等的是( )
| A. | NH4+和F- | B. | H3O+和CH4 | C. | O2-和Mg2+ | D. | Na+和 Cl- |
1.如图物品所使用的材料中,属于有机合成材料的是( )
| A. |  钛合金表链 | B. |  紫砂壶 | C. |  塑料保鲜盒 | D. |  真丝围巾 |
8.下列实验方案或做法不合理的是( )
| A. | 热固性塑料和热塑性塑料,可加热观察外形变化 | |
| B. | 用排水法收集O2结束时,先熄灭酒精灯,后移出导管 | |
| C. | 用稀H2SO4区别NaOH、K2CO3、BaCl2三种白色固体 | |
| D. | 为区别化肥硝酸钾和硝酸铵用加入熟石灰研磨闻气味 |
2. 同学,们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
同学,们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
【推理假设】上述两种物质发生反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
【实验探究】
(1)确定废液中是否含有盐酸:
①选择试剂:根据盐酸的化学性质,同学们选用了如图甲所示的五种物质,其中物质X是酸碱指示剂中的石蕊溶液.
②实验验证:某同学向废液中加入少量的镁粉,观察到无气泡产生,确定废液中一定没有盐酸.
(2)确定废液中是否含有Na2CO3:某同学选用pH试纸测出废液的pH=l0,确定废液中一定含有Na2CO3.
(3)处理废液,回收利用:欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
(4)拓展运用:
按图乙方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是Na2CO3.

 同学,们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.
同学,们用Na2CO3溶液和浓HCl来研究简易灭火器的反应原理时,对废液的成分进行探究.【推理假设】上述两种物质发生反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑,由此推测出废液中一定有NaCl,可能有Na2CO3或盐酸.
【实验探究】
(1)确定废液中是否含有盐酸:
①选择试剂:根据盐酸的化学性质,同学们选用了如图甲所示的五种物质,其中物质X是酸碱指示剂中的石蕊溶液.
②实验验证:某同学向废液中加入少量的镁粉,观察到无气泡产生,确定废液中一定没有盐酸.
(2)确定废液中是否含有Na2CO3:某同学选用pH试纸测出废液的pH=l0,确定废液中一定含有Na2CO3.
(3)处理废液,回收利用:欲从废液中得到纯净的NaCl,请完成如下实验方案设计.
| 方案 | 加入试剂 | 分离方法 | 方案评价 |
| 一 | 适量Ca(NO3)2溶液 | 过滤、蒸发结晶 | 不可行,理由是:引进新杂质 |
| 二 | 稍过量的盐酸 | 蒸发结晶 | 可行 |
按图乙方案分离BaCl2和NaCl的固体混合物时,X溶液中溶质是Na2CO3.


