题目内容
加热完全分解63.2g高锰酸钾,可以得到标准状态下的氧气多少升?(已知在标准状态下氧气的密度为1.43g/L,计算结果保留一位小数)
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,根据高锰酸钾的质量可以计算生成氧气的质量,进一步可以计算氧气的体积.
解答:解:设生成氧气的质量为x,
2KMnO4
K2MnO4+MnO2+O2↑,
316 32
63.2g x
=
,
x=6.4g,
可以得到标准状态下的氧气的体积为:6.4g÷1.43g/L=4.48L,
答:可以得到标准状态下的氧气4.48L.
2KMnO4
| ||
316 32
63.2g x
| 316 |
| 63.2g |
| 32 |
| x |
x=6.4g,
可以得到标准状态下的氧气的体积为:6.4g÷1.43g/L=4.48L,
答:可以得到标准状态下的氧气4.48L.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
用化学的观点解释下列成语,错误的是( )
| A、火上浇油:增加可燃物,使燃烧更剧烈 |
| B、釜底抽薪:将可燃物撤出燃烧区 |
| C、百炼成钢:逐渐降低生铁中碳、硅等含量 |
| D、花香四溢:说明分子可以再分 |
对于化学方程式2H2+O2
2H2O 表示的意义,叙述错误的是( )
| ||
| A、在点燃的条件下,氢气和氧气反应生成了水 |
| B、氢气加氧气反应生成水 |
| C、每4份质量的氢和32份质量的氧完全反应能生成36份质量的水 |
| D、在点燃的条件下,每二个氢气分子和一个氧分子化合生成二个水分子 |
小红同学的化学复习笔记本上有如下记录,你认为不准确的是( )
| A、化学反应发生时不一定能观察到明显的现象 |
| B、从物质的化学式可以判断物质中含有的元素 |
| C、配平化学方程式的依据是质量守恒定律 |
| D、一种元素只能组成一种单质 |
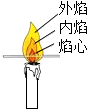 化学并不神秘,化学就在我们身边.只要我们采取适当的实验手段,留心观察,就能从司空见惯的事物中悟出很多科学道理.
化学并不神秘,化学就在我们身边.只要我们采取适当的实验手段,留心观察,就能从司空见惯的事物中悟出很多科学道理.