题目内容
6.归纳推理是学习化学的重要方法,以下说法中正确的是( )| A. | 单质是由同种元素组成的,所以由同种元素组成的物质都是单质 | |
| B. | CO2和CO的组成相同,所以它们的性质也相同 | |
| C. | 原子不显电性,所以构成原子的微粒也都不显电性 | |
| D. | 将燃着的木条伸入集气瓶中,木条熄灭,则集气瓶中的气体可能是二氧化碳 |
分析 A、由同种元素组成的物质不一定是单质,举出反例即可;
B、根据分子的性质进行分析;
C、根据原子核和核外电子所带电量的情况考虑;
D、将燃着的木条伸入瓶中,火焰立即熄灭,则说明该气体不能支持燃烧,据此由常见气体的性质进行分析判断.
解答 解:A、由同种元素组成的物质不一定是单质,如氧气与臭氧,故错误;
B、CO与CO2所含元素种类相同,但由于分子构成不同,所以它们的性质不完全相同,故错误;
C、原子核和核外电子所带电量相等,电性相反,所以整个原子不显电性,故错误;
D、将燃着的木条伸入到集气瓶中,木条熄灭,说明该气体不能燃烧、不能支持燃烧灭,该气体可能是氮气,也可能是二氧化碳等,故正确;
故选:D.
点评 解答本题要充分理解各种物质的性质方面的知识,只有这样才能对相关方面的问题做出正确的判断.

练习册系列答案
相关题目
14.如表列举的是通常状况下除去混合物中所含杂质的方法,其中正确的是( )
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | NaCl | Na2CO3 | 加过量稀盐酸、蒸发 |
| B | CO2 | H2O | 将混合气通过盛氢氧化钠固体的干燥装置 |
| C | FeSO4溶液 | CuSO4 | 加入足量锌粒,充分反应,过滤 |
| D | NaOH溶液 | Na2CO3 | 加入过量的Ca(OH)2溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.在一烧杯中盛有22.3g碳酸钠和氯化钠组成的固体混合物,加入109.1g水完全溶解.分四次向该溶液的烧杯中逐滴加入稀盐酸,每次均充分反应.实验数据记录如下:
请回答下列问题:
(1)写出所发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;.
(2)请根据已知条件列出求解恰好完全反应时,参加反应的固体质量(x)的比例式$\frac{106}{x}$=$\frac{44}{4.4g}$
(3)原混合物中氯化钠和碳酸钠质量的最简整数比117:106;
(4)该小组要用质量分数为36.5%浓盐酸配制上述所需的稀盐酸146g,则需浓盐酸的质量为20g;
(5)若恰好反应后所得溶液为不饱和溶液,则此时溶液的溶质质量分数为8.8%.
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 滴入稀盐酸的质量(g) | 36.5 | 36.5 | 36.5 | 36.5 |
| 反应后容器内物质总质量(g) | 165.7 | 200 | 236.5 | 273 |
(1)写出所发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑;.
(2)请根据已知条件列出求解恰好完全反应时,参加反应的固体质量(x)的比例式$\frac{106}{x}$=$\frac{44}{4.4g}$
(3)原混合物中氯化钠和碳酸钠质量的最简整数比117:106;
(4)该小组要用质量分数为36.5%浓盐酸配制上述所需的稀盐酸146g,则需浓盐酸的质量为20g;
(5)若恰好反应后所得溶液为不饱和溶液,则此时溶液的溶质质量分数为8.8%.
11.某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验. 
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.小聪则不同意小明的观点,他的理由是所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】空气中N2的含量计远大于O22的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2,请给出合理的解释:氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应.

(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律.小聪则不同意小明的观点,他的理由是所有的化学反应都遵循质量守恒定律.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象及结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝.证明猜想正确 |
18.如图为某反应的微观示意图,其中不同的球代表不同元素的原子,下列说法错误的是( )


| A. | 反应前后原子的种类和数目都不变 | |
| B. | 生成物可能都是氧化物 | |
| C. | 乙中元素的化合价在反应前后保持不变 | |
| D. | 反应物与生成物的分子个数比为1:1 |
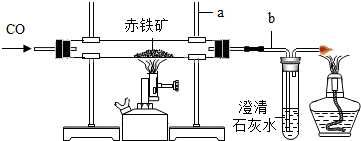 实验室模拟炼铁的实验装置如图所示,赤铁矿的主要成分是氧化铁(Fe2O3).
实验室模拟炼铁的实验装置如图所示,赤铁矿的主要成分是氧化铁(Fe2O3).