题目内容
7.元素周期律和周期表是学习化学的重要工具,如表是元素周期表的部分信息.
请认真分析表中信息,回答下列问题:
(1)地壳中含量最多的金属元素名称是铝,该元素原子的质子数为13.
(2)
 所表示的粒子符号为Mg2+,它的最外层电子数为8.
所表示的粒子符号为Mg2+,它的最外层电子数为8.(3)由原子序数为13和8的两种元素组成的化合物是Al2O3(写化学式).
分析 (1)根据地壳中含量最多的前五种元素考虑;(2)根据核内质子数大于核外电子数属于阳离子考虑;(3)根据化学式的书写方法考虑.
解答 解:(1)地壳中含量最多的前五种元素:氧、硅、铝、铁、钙,所以地壳中含量最多的金属元素名称是铝;该元素原子的质子数为13;
(2)质子数是12,属于镁元素,由于失去了两个电子变成了镁离子,即Mg2+,它的最外层电子数为8;
(3)原子序数为13是铝元素,原子序数为8是氧元素,所以化学式是:Al2O3;
故答案为:(1)铝;13;(2)Mg2+,8;(3)Al2O3;
点评 解答本题关键是要知道地壳中含量最多的前五种元素:氧、硅、铝、铁、钙;熟悉离子的写法,化学式的写法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12. 钒被誉为“合金中的维生素”,钒元素的部分信息如图.下列有关钒的说法正确的是( )
钒被誉为“合金中的维生素”,钒元素的部分信息如图.下列有关钒的说法正确的是( )
 钒被誉为“合金中的维生素”,钒元素的部分信息如图.下列有关钒的说法正确的是( )
钒被誉为“合金中的维生素”,钒元素的部分信息如图.下列有关钒的说法正确的是( )| A. | 属于非金属元素 | B. | 原子序数为23 | ||
| C. | 原子核外电子数为28 | D. | 相对原子质量为50.94g |
18.下列图象分别与选项中的操作相对应,其中不合理的是( )
| A. |  向一定量不饱和的硝酸钾溶液中不断加人硝酸钾晶体(不考虑温度变化) | |
| B. |  用等质量、等溶质质量分数的过氧化氢溶液制取氧气 | |
| C. |  一定条件下,一定质量的碳和氧气在密闭环境中反应 | |
| D. |  相同质量的镁粉和铁粉分别与过量且溶质质量分数相同的稀硫酸反应 |
2.我国已研究出C1O2的新制法,其反应的微观过程如图所示,下列说法正确的是( )

| A. | ClO2中氯元素的化合价为+5价 | |
| B. | 该反应中的各微粒是不运动的 | |
| C. | 该反应符合质量守恒定律 | |
| D. | 该反应的化学方程式为:2Cl+NaClO2=2ClO2+2NaCl |
12.规范的操作是实验成功的保证.下列实验操作正确的是( )
| A. |  CO2验满 | B. |  收集O2 | ||
| C. |  稀释浓硫酸 | D. |  测定溶液的派pH值 |
19.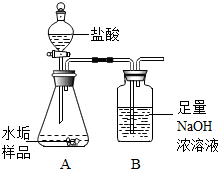 长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
分析上面实验与数据后,回答:
(1)第一次实验测得数据较低的原因是第一次实验生成的二氧化碳没有全部进入B装置中区去;
(2)平均每份水垢样品中碳酸钙的质量为多少克?(列出计算过程)
(3)水垢样品中氢氧化镁的平均质量分数为28.6%.(计算结果精确到0.1)
 长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:
长期使用的水壶底部都结有一层水垢,其主要成分是碳酸钙和氢氧化镁.为较准确测定水垢中氢氧化镁的含量,实验小组分别取三份同样的水垢样品各7.00g,利用右图所示装置连续进行三次实验,并将每次实验中装置B的质量变化记录于下表:| 第一次 | 第二次 | 第三次 | 平均值 | |
| B装置增加的质量(g) | 2.17 | 2.22 | 2.21 | 2.20 |
(1)第一次实验测得数据较低的原因是第一次实验生成的二氧化碳没有全部进入B装置中区去;
(2)平均每份水垢样品中碳酸钙的质量为多少克?(列出计算过程)
(3)水垢样品中氢氧化镁的平均质量分数为28.6%.(计算结果精确到0.1)

 如图是“×××”补钙剂商品标签图.我能根据标签信息完成下列问题:
如图是“×××”补钙剂商品标签图.我能根据标签信息完成下列问题: