题目内容
15.化学实验室要从X、银、铜、锌四种金属混合物中分离某贵重金属.流程如下:
请回答:
(1)四种金属的活动性顺序由强到弱的是Zn、X、Cu、Ag;
(2)固体丙中一定含有的金属是Ag;
(3)写出③中反应的化学方程式Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)为了检验滤液C中的溶质成分:向其中加入稀盐酸,有白色沉淀产生,则滤液C中一定含有的阳离子Ag+、Cu2+.
分析 根据金属能与酸反应的排在氢前面,不能与酸反应的排在氢的后面,活泼的金属能把不活泼的金属从盐溶液中置换出来分析金属活动性的顺序及反应过程中发生的反应并分析溶液中的成分.
解答 解:根据金属的活泼性顺序:锌>氢>铜>银,故向锌、X、铜、银的金属混合物中加入稀硫酸,锌一定参加反应产生气泡,而铜和银一定没反应,得到的滤液A再加入过量的锌得到混合物乙和滤液B,说明锌除了和过量的硫酸反应产生气体外,还和盐溶液发生了置换反应,因此说明锌的活动性比X强,且X位于氢前;由于硫酸过量,固体甲含有铜和银,铜和硝酸银反应产生硝酸铜和银,所以:
(1)四种金属的活动性顺序由强到弱的是:Zn、X、Cu、Ag;
(2)固体丙中一定含有的金属是被置换出的银及原有的银;
(3)③中是铜和硝酸银反应产生硝酸铜和银,化学方程式为;Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)向其中加入稀盐酸,有白色沉淀产生,说明有硝酸银剩余,所以滤液C中一定含有的阳离子是铜和硝酸银反应生成的铜离子和剩余的硝酸银中的银离子.
故答案为:(1)Zn、X、Cu、Ag;
(2)Ag;
(3)Cu+2AgNO3=Cu(NO3)2+2Ag;
(4)Ag+、Cu2+.
点评 本题以实验设计流程的形式让学生去利用金属活动性顺序表解决有关金属化学性质的问题,有一定的难度,解题的关键是熟练运用金属活动性的顺序意义.

练习册系列答案
相关题目
5.将浓盐酸和浓硫酸分别暴露在空气中,变化的结果是容器内( )
| A. | 酸液的质量都增大 | B. | 酸液的质量都减小 | ||
| C. | 酸液的浓度都增大 | D. | 酸液的浓度都减小 |
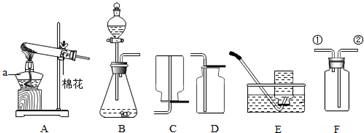
 化学课外小组设计了如图一套气体发生收集装置,以探究该装置的多功能性.
化学课外小组设计了如图一套气体发生收集装置,以探究该装置的多功能性.


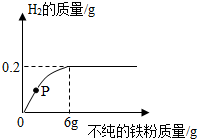 向一定量的稀盐酸中逐渐加入某种不纯的铁粉,加入铁粉的量与生成H2的关系如图所示,请回答有关问题:
向一定量的稀盐酸中逐渐加入某种不纯的铁粉,加入铁粉的量与生成H2的关系如图所示,请回答有关问题: