题目内容
5.将浓盐酸和浓硫酸分别暴露在空气中,变化的结果是容器内( )| A. | 酸液的质量都增大 | B. | 酸液的质量都减小 | ||
| C. | 酸液的浓度都增大 | D. | 酸液的浓度都减小 |
分析 根据物质的性质进行分析,浓盐酸具有挥发性,易挥发出溶质氯化氢而导致溶液变稀,浓硫酸具有吸水性,易吸收空气中的水分而使溶液变稀.
解答 解:A、将浓硫酸和浓盐酸分别暴露在空气中时,浓硫酸溶液的质量增大,浓盐酸的质量减小,该选项说法不正确;
B、将浓硫酸和浓盐酸分别暴露在空气中时,浓硫酸溶液的质量增大,浓盐酸的质量减小,该选项说法不正确;
C、将浓硫酸和浓盐酸分别暴露在空气中时,浓硫酸中,硫酸的质量不变,溶液质量增大,溶质质量分数减小,浓盐酸中,氯化氢的质量减小,溶液质量减小,溶质减小的质量和溶液减小的质量相等,溶质质量分数减小,该选项说法不正确;
D、将浓硫酸和浓盐酸分别暴露在空气中时,浓盐酸和浓硫酸的溶质质量分数都减小,该选项说法正确.
故选:D.
点评 浓盐酸、浓硫酸敞口放置时,它们的溶质的质量分数都会减小;但原因却不相同.浓盐酸是因其挥发性使溶质氯化氢的质量减小,从而使其中的溶质的质量分数减小;浓硫酸是因其吸水性使溶剂水的质量增大,从而使其中的溶质的质量分数减小.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
20.“分类”可以使人们有序的研究物质,以下分类正确的是( )
| A. | 金属材料:生铁、锰钢、焊锡 | B. | 碱:纯碱、烧碱、消石灰 | ||
| C. | 盐:氯化银、氯化钙、氯化氢 | D. | 合成材料:塑料、合成橡胶、铝合金 |
10.下列与含铁物质有关的化学方程式中,书写正确的是( )
| A. | 3Fe+2O2═Fe3O4 | B. | 2Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | FeCl3+NaOH═Fe(OH)3↓+NaCl | D. | Fe+CuSO4═FeSO4+Cu |
17.某烟气脱硫的工艺不仅能消除SO2,还能将其转化为石膏等产品,实现“变废为宝”,其主要物质转化关系如图所示,下列说法错误的是( )
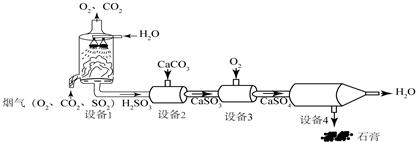

| A. | 设备1中发生的反应主要为SO2+H2O=H2SO3 | |
| B. | 流程图中能循环利用的物质是H2O | |
| C. | 设备3中反应前后各元素化合价均保持不变 | |
| D. | 该流程可有效减少酸雨的形成 |
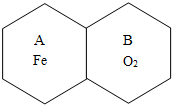 用四个六边形表示A(Fe)、B(O2)、C(CuSO4溶液)、D(P)四种物质,用相邻的六边形有共同的边表示两种物质可以发生反应,请回答下列问题
用四个六边形表示A(Fe)、B(O2)、C(CuSO4溶液)、D(P)四种物质,用相邻的六边形有共同的边表示两种物质可以发生反应,请回答下列问题