题目内容
6.造纸厂会产生含氢氧化钠的废水,须经处理呈中性后排放.为测定此废水中氢氧化钠的质量分数,小明取40g的废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,至恰好完全反应,消耗稀硫酸49g.计算废水中氢氧化钠的质量分数.(Na:23 O:16 H:1 S:32)分析 利用恰好完全反应所消耗硫酸的质量,根据反应的化学方程式,计算废水中氢氧化钠的质量;最后利用溶液中溶质的质量分数公式计算出废水中氢氧化钠的质量分数.
解答 解:反应消耗硫酸的质量为:49 g×10%=4.9 g
设废水样品中氢氧化钠的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 4.9 g
$\frac{80}{x}=\frac{98}{4.9g}$
x=4g
废水中氢氧化钠的质量分数为$\frac{4g}{40g}$×100%=10%
答:废水中氢氧化钠的质量分数为10%
点评 本题较简单,可直接利用化学方程式来计算,但应注意计算格式要规范,向规范要质量.

练习册系列答案
相关题目
17.关于下列三种粒子的说法正确的是( )


| A. | 表示同一种原子 | B. | Y显电中性 | C. | X表示阳离子 | D. | Z表示阴离子 |
1.下列选项中物质的名称,俗名,化学式不一致的是( )
| A. | 氧化钙 生石灰CaO | B. | 碳酸钠 纯碱 Na2CO3 | ||
| C. | 银 水银 Ag | D. | 氢氧化钠 苛性钠NaOH |
18.下列关于酸和碱的说法中不正确的是( )
| A. | 氢氧化钠、氢氧化钙的化学性质相似,是因为其溶液中含有金属离子 | |
| B. | 浓硫酸敞口放置一段时间后,其溶质质量分数减小 | |
| C. | 氢氧化钙常用于改良酸性土壤 | |
| D. | 氢氧化钠不能用于干燥二氧化碳气体 |
15. 长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量:将过量的稀盐酸加入到200g水垢中,同时测量3分钟内产生气体的质量,结果如下表:
长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量:将过量的稀盐酸加入到200g水垢中,同时测量3分钟内产生气体的质量,结果如下表:
试回答下列问题:
(1)表中有一个测量结果有较大的误差,这点对应的时间是120s.
(2)在右面坐标纸上,以反应时间为横轴、以产生的气体的质量为纵轴,画出产生气体的质量随反应时间变化的规
律的曲线图.
(3)计算水垢中碳酸钙的质量分数.
 长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量:将过量的稀盐酸加入到200g水垢中,同时测量3分钟内产生气体的质量,结果如下表:
长久使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,用稀盐酸可以清除水垢.某学校化学课外兴趣小组的同学通过实验测定水垢中碳酸钙的含量:将过量的稀盐酸加入到200g水垢中,同时测量3分钟内产生气体的质量,结果如下表:| 时间/s | 0 | 30 | 50 | 90 | 120 | 150 | 180 |
| 质量/g | 0 | 30 | 50 | 60 | 80 | 66 | 66 |
(1)表中有一个测量结果有较大的误差,这点对应的时间是120s.
(2)在右面坐标纸上,以反应时间为横轴、以产生的气体的质量为纵轴,画出产生气体的质量随反应时间变化的规
律的曲线图.
(3)计算水垢中碳酸钙的质量分数.
3.下列物质的性质中,属于物理性质的是( )
| A. | 鉴别真假黄金可用灼烧法 | B. | 物质挥发性 | ||
| C. | 物质可燃性 | D. | 物质氧化性 |
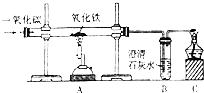 在实验室里,可以利用如图装置制得铁,请回答下列问题:
在实验室里,可以利用如图装置制得铁,请回答下列问题: