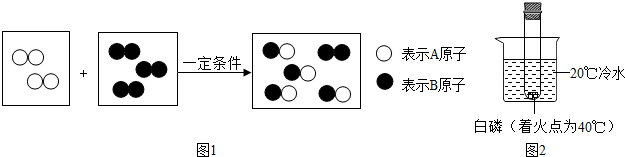
题目内容
15.下列离子在pH=1的溶液中能够大量共存的是( )| A. | SO42-、Na+、K+、Cl- | B. | Ca2+、K+、Cl-、CO32- | ||
| C. | Fe2+、CO32-、K+、Cl- | D. | Al3+、Ag+、K+、Cl- |
分析 根据pH=1的无色溶液,并利用复分解反应发生的条件,离子不能结合生成水、气体、沉淀来分析解答.
解答 解:A、四种离子在酸性环境中不能结合成水、气体或沉淀,故正确;
B、在酸性条件下,H+与CO32-结合生成水和二氧化碳,Ca2+与CO32-能结合生成碳酸钙沉淀,不能共存,故错误;
C、在酸性条件下,H+与CO32-结合生成水和二氧化碳,不能共存,故错误;
D、Cl-与Ag+能结合生成氯化银沉淀,不能大量共存,故错误;
故选项为:A.
点评 本题考查离子的共存问题,注意PH=1、无色溶液等信息的使用,学生需熟悉复分解反应发生的条件、物质的溶解性等.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
3.将镁条放入盛有硫酸铜溶液的试管中,可以观察到镁条表面析出紫红色固体的同时有气泡产生,用点燃的火柴试验该气体,能产生微弱的淡蓝色火焰,同时可听到轻微的爆鸣声.小黄同学就该实验现象的一些推论正确的是( )
| A. | 硫酸铜溶液在物质分类上属于化合物中的盐类 | |
| B. | 由轻微的爆鸣声可知有氢气生产,说明该硫酸铜溶液中一定混入某种酸溶液 | |
| C. | 用点燃的火柴试验,能产生微弱的淡蓝色火焰,说明该气体的主要性质是还原性 | |
| D. | 镁条放入硫酸铜溶液中有气泡产生,可以大胆推测硫酸铜溶液可能呈酸性 |
20.每年的4月22日是“世界地球日”,2015年地球日的活动主要为“珍惜地球资源 转变发展方式-提高资源利用效益”.下列做法不符合活动主题的是( )
| A. | 农业和园林灌溉,改大水浸灌为喷灌、滴灌 | |
| B. | 改进汽车发动机的燃烧方式,使汽油充分燃烧 | |
| C. | 为提高粮食产量,大量使用各种化肥、农药 | |
| D. | 回收利用废旧金属、废旧书籍及废弃废弃塑料 |
5.氢氧化钠的氢氧化钙是两种常见的碱,李红同学将两种碱的溶液分别装入试管A,B中,并进行了如图所示的三组实验.
(1)实验1中,两支试管的溶液都变成红色.
(2)实验2中,若B盛装的是NaOH溶液,发生反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4,该反应的基本类型是复分解反应.
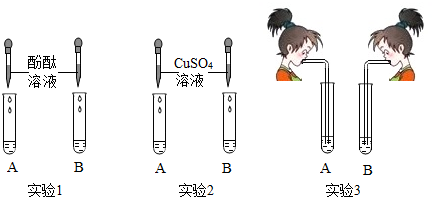
(3)实验3中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,B中无现象,为了探究吹气后B中溶质的成分,李红进行了如下探究:
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
…
实验和结论:
反思与评价:
老师评价李红得出的结论不正确,是因为猜想2(填数字)也会产生相同的现象.如果要验证“猜想3成立”,必需更换试剂,将氢氧化钙溶液换成氯化钙溶液.
(1)实验1中,两支试管的溶液都变成红色.
(2)实验2中,若B盛装的是NaOH溶液,发生反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4,该反应的基本类型是复分解反应.

(3)实验3中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O,B中无现象,为了探究吹气后B中溶质的成分,李红进行了如下探究:
提出猜想:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
…
实验和结论:
| 实验 | 实验现象 | 结论 |
| 取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液 | 产生白色沉淀溶液呈现红色 | 猜想3成立 |
老师评价李红得出的结论不正确,是因为猜想2(填数字)也会产生相同的现象.如果要验证“猜想3成立”,必需更换试剂,将氢氧化钙溶液换成氯化钙溶液.