题目内容
11.学习化学离不开实验,试回答下列问题:(1)如图所示是初中化学常见的实验装置图,请回答:
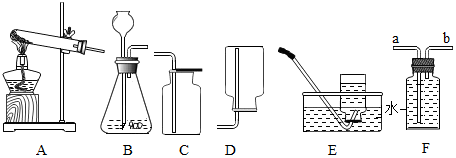
①实验室用B装置制取氧气,反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;若用E装置收集的氧气不纯,则可能的原
因是未等气泡连续均匀冒出时收集(合理均可)(答出一种即可);若用F装置收集氧气,气体应从b(填“a”或“b”)端进入;
②实验室制取并收集一瓶二氧化碳气体,应选用的装置为BC(填字母序号),在装入药品
前应先检查装置的气密性.
(2)用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“一定溶质质量分数氯化钠溶液的配制”两个实验.
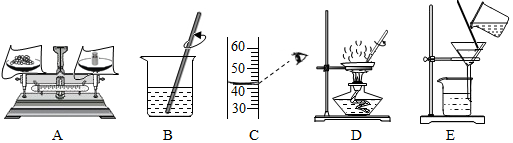
①操作E中得到的滤液仍浑浊,其原因可能是滤纸破损(合理均可)(答出一点即可);
②若图B所用的烧杯内壁沾有水,会导致所配氯化钠溶液中溶质的质量分数偏小(填“偏大”、“偏小”或“不变”);
③图D中玻璃棒的作用是搅拌,防止液体局部温度过高液滴飞溅;
④图C中有一处明显的错误,请你改正:视线与凹液面最低处相平.
分析 (1)①B装置属于固液常温型,利用过氧化氢制取氧气可用此发生装置,据反应原理书写方程式;并结合排水法收集气体、氧气密度比水小分析解答;
②实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,故 选发生装置B,二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集,装入药品前要检查装置气密性,防止装置漏气;
(2)①过滤后滤液浑浊的原因可能有滤纸破损、液面高于滤纸边缘、仪器不干净;
②据溶质的质量分数计算方法分析解答;
③蒸发时玻璃棒的作用是搅拌,防止液体局部温度过高液滴飞溅;
④利用量筒量取液体时正确的读数方法是视线与凹液面的最低处保持水平.
解答 解:(1)①B装置属于固液常温型,利用过氧化氢制取氧气可用此发生装置,反应的化学方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;用E装置收集的氧气不纯,可能是集气瓶内未装满水、也可能是 未等气泡连续均匀冒出时收集,导致集气瓶内混入了空气;氧气密度比水小,所以用F装置收集氧气时应从短管进气,长管便于排水;
②实验室制取二氧化碳用大理石和稀盐酸常温反应,属于固液常温型,故 选发生装置B,二氧化碳密度比空气大且能溶于水,所以用向上排空气法收集,装入药品前要检查装置气密性,防止装置漏气;
(2)①过滤后滤液浑浊的原因可能有滤纸破损、液面高于滤纸边缘、仪器不干净;
②若图B所用的烧杯内壁沾有水,则所配溶液中溶剂的质量增加,溶质的质量分数=$\frac{溶质的质量}{溶液的质量}$×100%,所以会导致所配氯化钠溶液中溶质的质量分数偏小;
③蒸发时玻璃棒的作用是搅拌,防止液体局部温度过高液滴飞溅;
④图C俯视读数,利用量筒量取液体时正确的读数方法是视线与凹液面的最低处保持水平;
故答案为:(1)①2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑; 未等气泡连续均匀冒出时收集(合理均可); b;
②BC; 检查装置的气密性;
(2)①滤纸破损(合理均可); ②偏小; ③搅拌,防止液体局部温度过高液滴飞溅;④视线与凹液面最低处相平.
点评 本题主要考查了实验室制取气体的反应原理、装置选取、注意事项,及一些基本的实验操作,掌握相关知识和必要的操作技能是解答此题的关键.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(1)首先制取碳酸氢铵:NH3+CO2+H2O=NH4HCO3,该反应的基本反应类型为化合反应.
(2)第二步是用食盐与NH4HCO3反应.原料食盐来源于的渤海湾,从海水中提取粗盐.该粗盐主要含有氯化钠,还含有少量的氯化钙、氯化镁和硫酸钠.为得到纯净的食盐水将粗盐水进行如下净化过程:
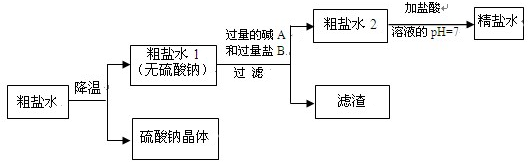
①从粗盐水中析出硫酸钠晶体其原理是降温结晶
②碱A 是由郊县的石灰石资源得到的,则过量的碱A 和粗盐水中的物质反应的方程式为Ca(OH)2+MgCl2=CaCl2+Mg(OH)2↓
③加入的盐B 是,滤渣中含有的物质是Mg(OH)2、CaCO3
④查阅资料得知NaCl、NH4HCO3、NaHCO3、NH4Cl 在30℃时的溶解度如表所示:
| 温度 | NH4Cl | NH4HCO3 | NaHCO3 | NaCl |
| 30℃ | 41.1g | 27.0g | 11.1g | 36.3g |
(3)第三步加热碳酸氢钠:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
| A. |  读液体体积 | B. |  吸取稀盐酸 | ||
| C. |  熄灭酒精灯 | D. |  向试管中装入锌粒 |
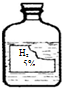 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少 量二氧化锰粉末. | 没有气泡产生. | 该液体不是过氧化氢溶液. |
| 步骤二:取该液体适量于试管中,向其中滴加少量硝酸钡溶液. | 有白色沉淀生成 | 该液体是稀硫酸. |
| A. | 涤纶和羊毛,点燃都闻到烧焦羽毛气味 | |
| B. | 大风吹灭蜡烛火焰,降低蜡烛的着火点 | |
| C. | 缺少微量元素硒,大量食用含硒营养剂 | |
| D. | 蒸馏和煮沸,均可将硬水转化为软水 |
| A. | 用含小苏打的发酵粉焙制糕点 | B. | 合理使用食品添加剂NaNO2 | ||
| C. | 用霉变的花生做鱼皮豆 | D. | 合理使用加碘盐 |

| A. | ③④元素的化学性质相似 | |
| B. | ②④粒子核外电子排布相同 | |
| C. | ②④都具有相对稳定结构,但是②是原子而④是离子 | |
| D. | ③属于金属元素的原子 |
第Ⅰ组实验:取5只集气瓶,编号为①、②、③、④、⑤,分别装入其总容积50%、40%、30%、20%、10%的饱和碳酸氢钠溶液,用排液法收集五瓶CO2气体(如图所示).然后,将燃着的木条依次插入①~⑤号瓶中,记录实验现象.
| 第Ⅰ组 | 第Ⅱ组 | 第Ⅲ组 | |||||||||
| 集气瓶编号 | ① | ② | ③ | ④ | ⑤ | ① | ② | ③ | ④ | ⑤ | ① |
| CO2占容积的体积分数(%) | 50 | 40 | 30 | 20 | 10 | 29 | 27 | 25 | 23 | 21 | 28 |
| 木条燃烧情况 | 熄灭 | 熄灭 | 熄灭 | 时燃 时灭 | 安静 燃烧 | 熄灭 | 时燃 时灭 | 时燃 时灭 | 时燃 时灭 | 时燃 时灭 | 熄灭 |
见上表.请跟据实验回答下列问题:
(1)如图标示仪器①的名称是烧杯,实验室制取CO2的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.请你推测为何用排碳酸氢
钠饱和溶液的方法收集CO2,而不用排水法收集CO2在碳酸氢钠溶液中溶解度很小,而却能溶于水.
(2)实验室常用澄清石灰水来鉴别CO2气体.
(3)收集的CO2占容积的体积分数最低为28%时,可使燃着的木条熄灭.

注意:下面的问题你若继续回答且正确本题另奖励4分,本试卷总分不超过60分
(4)采取“半值法”探究能减少实验次数.例如:第Ⅰ组实验若按③、④的编号顺序进行实验,即可确定下一组实验收集的CO2占容积的体积分数应在20%~30%之间,从而省去编号为①②⑤;的实验.同理,第Ⅱ组实验可以省去的实验编号为③④⑤.