题目内容
6. 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少 量二氧化锰粉末. | 没有气泡产生. | 该液体不是过氧化氢溶液. |
| 步骤二:取该液体适量于试管中,向其中滴加少量硝酸钡溶液. | 有白色沉淀生成 | 该液体是稀硫酸. |
分析 根据过氧化氢能在二氧化锰的催化作用下快速的生成氧气,硫酸能够和氯化钡等产生白色沉淀分析;
解答 解:步骤一:根据该液体不是过氧化氢溶液的结论,所以是向液体中加入二氧化锰验证不是过氧化氢溶液,没有气泡产生;
步骤二:该液体是稀硫酸和氯化钡反应产生硫酸钡白色沉淀;
故答案为:步骤一:二氧化锰;步骤二:有白色沉淀生成
点评 本题考查了破损标签试剂的确定,完成此题,可以依据破损标签的部分以及有关物质的性质进行.要求同学们熟练掌握有关物质的性质,以便灵活应用.

练习册系列答案
相关题目
1.分析处理图表中的信息是学习化学的一种重要方法.
(1)表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
①40℃时,氯化钠的溶解度为36.6g.
②碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将 100g 的水加入 30g 碳酸钠中,充分搅拌后得到的是饱和溶液(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到 30℃,该溶液的溶质质量分数为23.1% (计算结果精确到 0.1%).
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是碳酸钠饱和溶液.
(2)将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式Fe+2HCl=FeCl2+H2↑.如图是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是AC(填标号).
(1)表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
| 温度/℃ | 10 | 20 | 30 | 40 | |
| 溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
| 碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
②碳酸钠的溶解度随温度的升高而增大(填“增大”或“减小”).在20℃时,将 100g 的水加入 30g 碳酸钠中,充分搅拌后得到的是饱和溶液(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到 30℃,该溶液的溶质质量分数为23.1% (计算结果精确到 0.1%).
③10℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是碳酸钠饱和溶液.
(2)将足量的稀盐酸加入一定量的铁、铜混合物中,写出其中反应的化学方程式Fe+2HCl=FeCl2+H2↑.如图是实验过程生成气体或剩余固体的质量随反应时间的变化关系,其中表示正确的是AC(填标号).

17.下列推理或实验结论正确的是( )
| A. | 蔗糖、葡萄糖等有甜味,则糖类物质都有甜味 | |
| B. | 化学变化中原子、离子都不会改变 | |
| C. | 可以用取样灼烧的方法区别蚕丝和棉纱线 | |
| D. | 某化肥中加熟石灰研磨,未闻到氨臭气味,该化肥一定不是氮肥 |
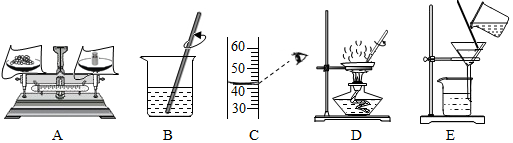
18.利用铜和浓硫酸反应,制取二氧化硫和硫酸铜晶体,能达到实验目的是( )


| A. | 用图甲装置制取并收集二氧化硫 | |
| B. | 用图乙装置向反应后的混合物中加水稀释 | |
| C. | 用图丙装置过滤出稀释后混合物中的不溶物 | |
| D. | 用图丁装置将硫酸铜溶液蒸发浓缩后冷却结晶 |
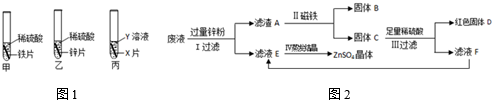
15.下列关于金属制品的使用,方法合理的是( )
| A. | 铝合金门窗变暗后用砂纸打磨 | B. | 在铁桶中配制农药波尔多液 | ||
| C. | 尝试用锡来做灯丝 | D. | 切菜刀用后及时冲洗晾干 |
16.下列实验现象描述不正确的是( )
| A. | 稀盐酸除铁锈,铁锈逐渐消失,溶液逐渐由无色变为黄色 | |
| B. | 纯铁钉放入硝酸银溶液中,铁钉表面有银白色物质析出,溶液由无色逐渐变为浅绿色 | |
| C. | 氢氧化钡溶液和硫酸铜溶液混合,同时产生白色沉淀和蓝色沉淀 | |
| D. | 细铁丝在空气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体 |