题目内容
13.取镁、锌、铁三种金属分别与足量盐酸反应.(1)若反应后各生成氢气30g,则需要这三种金属的质量各是多少?
(2)试推断,相同质量的镁、锌、铁分别与足量的盐酸充分反应,生成氢气的质量比是多少?
分析 锌和稀盐酸反应生成氯化锌和氢气,铁和稀盐酸反应生成氯化亚铁和氢气,镁和稀盐酸反应生成氯化镁和氢气,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)设需要镁、锌、铁的质量分别为x、y、z,
Mg+2HCl═MgCl2+H2↑,Zn+2HCl═ZnCl2+H2↑,Fe+2HCl═FeCl2+H2↑,
24 2 65 2 56 2
x 30g y 30g z 30g
$\frac{24}{x}$=$\frac{2}{30g}$,$\frac{65}{y}$=$\frac{2}{30g}$,$\frac{56}{z}$=$\frac{2}{30g}$,
x=360g,y=975g,z=840g,
答:若反应后各生成氢气30g,则需要这三种金属的质量各是360g、975g、840g.
(2)设镁、锌、铁的质量都是m,
Mg+2HCl═MgCl2+H2↑,Zn+2HCl═ZnCl2+H2↑,Fe+2HCl═FeCl2+H2↑,
24 2 65 2 56 2
m $\frac{2}{24}$m m $\frac{2}{65}$m m $\frac{2}{56}$m
相同质量的镁、锌、铁分别与足量的盐酸充分反应,生成氢气的质量比是:$\frac{2}{24}$m:$\frac{2}{65}$m:$\frac{2}{56}$m=65:24:56,
答:相同质量的镁、锌、铁分别与足量的盐酸充分反应,生成氢气的质量比是65:24:56.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 10% | B. | 20% | C. | 40% | D. | 5% |
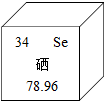 茄子营养丰富,其中含有水、糖类、蛋白质、胡萝卜素、维生素B、维生素C、维生素E以及钾、钙、磷、铁、锌、硒等元素.
茄子营养丰富,其中含有水、糖类、蛋白质、胡萝卜素、维生素B、维生素C、维生素E以及钾、钙、磷、铁、锌、硒等元素. A、B、C、D、E是初中化学中常见的五种物质.在通常情况下,A为黑色粉末状固体,B、C均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取C,单质E是组成空气的主要成分之一.它们之间的关系如图所示(图中反应条件及反应④和⑤中某些反应物、生成物已略去).
A、B、C、D、E是初中化学中常见的五种物质.在通常情况下,A为黑色粉末状固体,B、C均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取C,单质E是组成空气的主要成分之一.它们之间的关系如图所示(图中反应条件及反应④和⑤中某些反应物、生成物已略去).
 水是人类宝贵的自然资源
水是人类宝贵的自然资源