题目内容
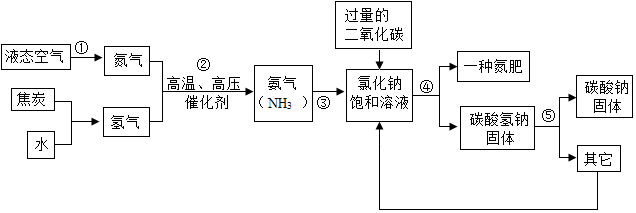
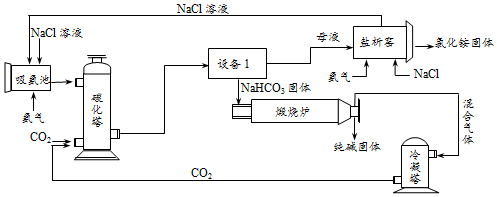
6.现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:
已知:贝壳的主要成分是CaCO3
反应②的化学方程式为:NaCl(饱和溶液)+NH3+H2O+CO2═NH4Cl+NaHCO3↓
(1)反应①的另一种产物是配制石灰乳的主要原料之一,配制石灰乳时发生反应的化学方程式为CaO+H2O═Ca(OH)2.
(2)反应③的基本反应类型是分解反应,反应的化学方程式为2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)母液中含有的溶质是NH4Cl、NaHCO3.
(4)整个生产过程中可循环利用的物质是CO2、NH3.
分析 (1)根据化学方程式的书写方法进行分析;
(2)根据化学方程式的书写方法以及反应类型的有关知识进行分析;
(3)析出晶体后的母液中含有NaHCO3、NH4Cl,据此分析;
(4)根据反应前后的物质推出可以循环利用的物质即可.
解答 解:(1)碳酸钙在高温的条件下分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,因此配制石灰乳时发生反应的化学方程式为CaO+H2O═Ca (OH)2.
(2)碳酸氢钠受热分解生成了碳酸钠、二氧化碳和水,反应的方程式是:2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.该反应由一种物质生成了三种物质,属于分解反应.
(3)析出晶体后的母液中含有NaHCO3、NH4Cl.
(4)通过分析反应原理可知,氨气、二氧化碳既是反应物,也是生成物,所以整个流程中可以循环利用的物质是NH3、CO2.
故填:(1)CaO+H2O═Ca (OH)2;(2)分解反应;2NaHCO3 $\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑;(3)NH4Cl、NaHCO3;(4)CO2、NH3.
点评 本题难度不大,以“侯氏制碱法”模拟流程图为素材,考查了化学方程式的书写方法、反应类型等,掌握反应类型知识、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.X、Y两元素的相对原子质量之比为7:2,X与Y形成的化合物中,X、Y两元素的质量之比为21:8,则该化合物的化学式可表示为( )
| A. | X3Y2 | B. | X3Y4 | C. | X2Y3 | D. | XY |
14.下列叙述正确的是( )
| A. | 鱼类能在水中生活,证明氧气易溶于水 | |
| B. | 硫在氧气中燃烧,火焰呈淡蓝色 | |
| C. | 氧气可以支持燃烧,说明氧气具有可燃性 | |
| D. | 农家肥的腐熟,食物腐烂都是缓慢氧化的结果 |
11.分子、原子等粒子构成物质,用我们所学的分子、原子的相关知识解释下列现象,正确的是( )
| A | 热胀冷缩是因为分子或原子的大小发生改变 |
| B | 美酒飘香,是由于分子在不断运动 |
| C | 冰冻三尺非一日之寒,水结冰时,分子静止不动 |
| D | 空气中的氧气、二氧化碳经混合,它们的化学性质改变 |
| A. | A | B. | B | C. | C | D. | D |