题目内容
11.分子、原子等粒子构成物质,用我们所学的分子、原子的相关知识解释下列现象,正确的是( )| A | 热胀冷缩是因为分子或原子的大小发生改变 |
| B | 美酒飘香,是由于分子在不断运动 |
| C | 冰冻三尺非一日之寒,水结冰时,分子静止不动 |
| D | 空气中的氧气、二氧化碳经混合,它们的化学性质改变 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,结合事实进行分析判断即可.
解答 解:A、分子或原子间有间隔,受热时物质分子或原子间的间隔增大,遇冷时间隔缩小,分子或原子的大小没有改变,故选项解释错误.
B、美酒飘香,是因为酒香中含有的分子是在不断运动的,向四周扩散,使人闻到酒的气味,故选项解释正确.
C、分子总在不停的运动,水结冰时,分子也在运动,只是运动速率慢了,故选项解释错误.
D、空气中氧气、二氧化碳经混合后没有发生化学变化,分子都保持原来的性质,它们的化学性质都没有发生改变,故选项解释错误.
故选:B.
点评 本题难度不大,掌握分子的基本性质及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
相关题目
19.小苏打(碳酸氢钠)在日常生活中有广泛的用途,工业上制取小苏打有多种方法,其中有一种是气相固碳法,其利用的原理是:Na2CO3+H2O+CO2=2NaHCO3
资料1:NaHCO3+NaOH=Na2CO3+H2O
资料2:碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下)(部分)
学校实验小组验证反应原理,在室温为15℃时,同学们将10g氢氧化钠固体完全溶解溶于80g水中(见图1烧杯),而后匀速的通入二氧化碳气体.同时用传感器测定溶液的pH变化,同时用数据采集器记录并绘制图象如图2所示.
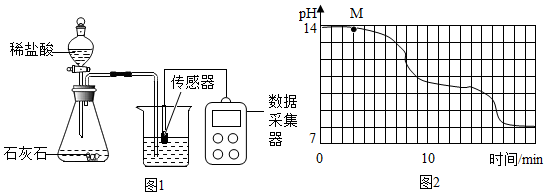
(1)图1所示实验中,用“分液漏斗”而不用“长颈漏斗”其原因是控制稀盐酸滴入速率,从而控制二氧化碳生成速率;
(2)通过图象分析,小苏打溶液是显碱性(填“酸性”、“中性”或“碱性”),图象中M点处发生的主要化学反应方程式为2NaOH+CO2=Na2CO3+H2O;
(3)为了确定M处溶液的成分,同学们进行如下实验:
(4)实验过程中,同学们发现18min后溶液的pH基本不再变化,则此时烧杯中就可观察到的现象有出现白色不溶物.
资料1:NaHCO3+NaOH=Na2CO3+H2O
资料2:碳酸钠和碳酸氢钠的溶解度表(一个标准大气压下)(部分)
| 温度/℃ | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
| 碳酸氢钠溶解度/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
| 碳酸钠溶解度/g | 7.7 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |

(1)图1所示实验中,用“分液漏斗”而不用“长颈漏斗”其原因是控制稀盐酸滴入速率,从而控制二氧化碳生成速率;
(2)通过图象分析,小苏打溶液是显碱性(填“酸性”、“中性”或“碱性”),图象中M点处发生的主要化学反应方程式为2NaOH+CO2=Na2CO3+H2O;
(3)为了确定M处溶液的成分,同学们进行如下实验:
| 实验步骤 | 加入试剂 | 实验现象 | 初步实验结论 |
| ① | 加入 足量氯化钙溶液 | 有白色沉淀 | 有碳酸钠和氢氧化钠物质 |
| ② | 滴入 酚酞试液 | 酚酞试液变红色 |
16.物质的用途与性质密切相关,下列说法错误的是( )
| A. | 铜用于制导线,是由于铜有良好的导电性 | |
| B. | 二氧化碳能够灭火,是由于其不燃烧、不支持燃烧,且密度比空气大 | |
| C. | 氮气常用作保护气,是由于氮气的化学性质稳定 | |
| D. | 铁制品表面涂“银粉”(铝粉),是由于铝的化学性质比铁稳定 |
3.下列说法不正确的是( )
| A. | 决定元素种类的是质子数 | |
| B. | 氧气难溶于水 | |
| C. | 二氧化锰可以做过氧化氢分解的催化剂 | |
| D. | 鉴别硬水与软水可以用肥皂水 |
1.2017年的5月30日是传统节日“端午节”.“五月端午粽飘香”,糯米是粽子的主要食材,其主要成分是( )
| A. | 淀粉 | B. | 油脂 | C. | 蛋白质 | D. | 维生素 |


