题目内容
20.随着人们生活水平的不断提高,汽车已走进千家万户.制造汽车要用到含铜、铁、铝等成分的多种金属材料.(1)在汽车电路中,经常用铜作导线,这是利用了铜的导电性.
(2)车体多用钢材制造.其表面喷漆不仅美观,而且可有效防止与水和氧气接触而生锈.
(3)工业上用CO还原赤铁矿冶炼金属铁的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)在实验室中探究锌、铜的金属活动性顺序,除锌、铜外,还需要用到的试剂是盐酸.(填一种即可)请根据选定的试剂写出上述实验中发生反应的一个化学方程式Zn+2HCl═ZnCl2+H2↑.
分析 根据物质的性质进行分析解答,一氧化碳能与氧化铁高温反应生成铁和二氧化碳,根据金属活动性顺序以及化学方程式的书写进行分析解答即可.
解答 解:(1)铜具有导电性,能用作导线,故填:导电;
(2)在铁表面喷漆能防止铁与水和氧气接触而防锈,故填:水和氧气;
(3)一氧化碳与氧化铁高温反应生成铁和二氧化碳,故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(4)要验证锌和铜的活动性,可以使用稀盐酸,锌能与盐酸反应生成氯化锌和氢气,而铜不反应,故填:盐酸;Zn+2HCl═ZnCl2+H2↑.
点评 本题考查的是金属的性质,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
8.下列家庭实验不会成功的是( )
| A. | 用缝衣针淬火处理后制钓鱼钩 | |
| B. | 用6B铅笔芯做导电性实验 | |
| C. | 用等质量的同种白糖加入等量热水与冷水中,比较溶解速率 | |
| D. | 用冷碟子放在蜡烛火焰上制取炭黑 |
5.专家介绍,患者一旦确诊为人感染H7N9禽流感病毒病例,可以马上使用“达菲”等抗病毒药物进行治疗.合成“达菲”的主要原料莽草酸(化学式为 C7H10O5)存在于我国盛产的八角茴香中.下列说法不正确的是( )
| A. | 莽草酸中碳、氢、氧三种元素的质量比为42:5:40 | |
| B. | 莽草酸的相对分子质量为87 | |
| C. | 每个莽草酸分子中含有22个原子 | |
| D. | 莽草酸中碳元素的质量分数约为21% |
12.根据表中的数据,回答下列问题.
(1)20℃时,称取31.6g 硝酸钾固体加入盛有100g水的烧杯中,充分溶解形成的溶液是饱和(填“饱和”或“不饱和”)溶液;
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法为降温结晶
(3)将等质量硝酸钾的饱和溶液和氯经钠的饱和溶液从60℃降温到20℃,对所得溶液的叙述正确的是AC(填序号)
A、都是饱和溶液 B、溶剂质量:硝酸钾>氯化钠 C、溶液质量:硝酸钾<氯化钠.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/ | 氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 | |
(2)当硝酸钾中混有少量氯化钠时,提纯硝酸钾所采用的方法为降温结晶
(3)将等质量硝酸钾的饱和溶液和氯经钠的饱和溶液从60℃降温到20℃,对所得溶液的叙述正确的是AC(填序号)
A、都是饱和溶液 B、溶剂质量:硝酸钾>氯化钠 C、溶液质量:硝酸钾<氯化钠.
10.老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
(1)①此气体是什么物质?验证它的实验方案如下:
②我想制取该气体,发生装置将选取下图中的B 收集装置选取C(或E).
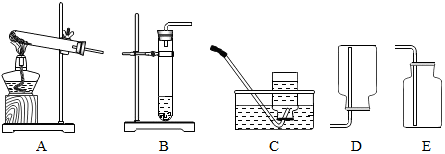
(1)①此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可能是 氧气 | ||
| 产生此气体的一个化学方程式是 | ||
