题目内容
15.已知反应A+3B=3C,取7gA和一定量的B完全反应,可生成8.5gC,则A和B的相对分子质量之比为14:1.分析 根据化学方程式的意义进行分析,化学反应中各物质的质量比是定值,据此解答即可.
解答 解:7克A和一定量的B完全反应生成8.5克C,根据质量守恒定律,则B的质量为:8.5g-7g=1.5g,设A、B的相对分子质量为x、y
A+3B═3C
x 3y
7g 1.5g
$\frac{x}{7g}=\frac{3y}{1.5g}$
故x:y=14:1
故填:14:1.
点评 本题考查了根据化学方程式的计算,此题的易错点是在向方程式中代入物质的质量时易与化学计量数相乘.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
6.以下图象关系表示正确的是( )
| A. |  向盐酸中不断加入水 | |
| B. |  向接近饱和的NaCl溶液中加入NaCl固体 | |
| C. | 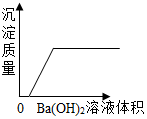 向含有H2SO4的CuSO4溶液中滴入Ba(OH)2溶液 | |
| D. | 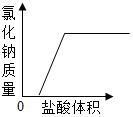 向久置空气中的NaOH溶液加入盐酸 |
7.下列物质溶液中,若滴入酚酞试液变红色,若滴入氯化铜溶液则产生蓝色沉淀,若加入碳酸钠溶液有白色沉淀生成,若通入二氧化碳气体,溶液呈白色混浊,该溶液可能是( )
| A. | 氢氧化钙溶液 | B. | 氢氧化钠溶液 | C. | 氢氧化钡溶液 | D. | 氯化钙溶液 |
4.为测定纯碱样品中Na2CO3的含量(杂质不溶于水,也不溶于酸、碱溶液).小雨同学设计了这样一个方案:将一包样品分成质量相等的两份,向其中一份加入适量的Ca(OH)2溶液,充分反应后,得到10.3g不溶物质;向另一份中加入足量的盐酸溶液,充分反应后,得到2.2g气体.则纯碱样品中Na2CO3的含量是( )
| A. | 50% | B. | 74.2% | C. | 96.4% | D. | 94.6% |
5.下列实验现象描述正确的是( )
| A. | 蜡烛在空气中燃烧生成二氧化碳和水 | |
| B. | 红磷在空气中燃烧,产生大量白色烟雾 | |
| C. | 木炭在氧气中燃烧,发出黄色火焰,生成有刺激性气味的气体 | |
| D. | 氢气在空气中燃烧,产生淡蓝色的火焰 |

 如图为“一氧化碳与氧化铁反应”的实验装置.
如图为“一氧化碳与氧化铁反应”的实验装置.