题目内容
19.造纸是我国古代四大发明之一,它有效地推动了人类文明的发展.(1)回收农田产生的秸秆作为造纸原料.秸秆的主要成分是纤维素[(C6H10O5)n],纤维素中C、H、O三种元素的质量比为36:5:40(用最简整数比表示).
(2)某校综合实践小组的同学用溶质质量分数为10%的稀盐酸溶液,对一造纸厂排放的NaOH的碱性废水进行检测.请问用质量分数为37%的浓盐酸配制质量分数为10%的稀盐酸100g,配制的步骤依次为计算、量取、稀释、转移装瓶.
(3)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后排放.若某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸196g (H2SO4的质量分数为20%),可以处理造纸厂的废水质量是多少?(写出完整的计一算过程)
分析 (1)化学式中各元素的质量比为各元素的相对原子质量×原子个数的之比,据此分析计算回答.
(2)将浓盐酸稀释为稀盐酸的步骤是;计算、量取、稀释、装瓶;
(3)可先根据化学方程式求出氢氧化钠的质量,再根据废水中氢氧化钠的质量分数求出废水的质量.
解答 解:
(1)根据纤维素的化学式(C6H1005)n知,纤维素中C、H、O三种元素的质量比=(12×6):(1×10):(16×5)=36:5:40.
(2)用质量分数为37%的浓盐酸配制质量分数为10%的稀盐酸100g,配制的步骤依次为计算需要浓盐酸的质量、进而计算其体积,然后用量筒量取浓盐酸、水,并混合稀释溶解,装瓶;
(3)196g废硫酸溶液中含硫酸的质量为196g×20%=3920g
设196g废硫酸溶液可以反应氢氧化钠的质量为x
H2SO4 +2NaOH=Na2SO4 +2H2O
98 80
3920g x
$\frac{98}{80}$=$\frac{3920g}{x}$
x=320g
则需要氢氧化钠的废水的质量=$\frac{320g}{1.6%}$=2000g
故答案为:
(1)36:5:40;(2)量取;稀释;(3)答:可以处理的废水质量是2000g.
点评 本题主要考查化学式的含义、溶液配制及根据化学方程式进行简单计算的能力.难度不大,根据已有的知识即可分析解答.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
9.下列物品所使用的材料中,不属于有机合成材料的是( )
| A. | 有机玻璃 | B. | 钢化玻璃 | C. | 合成橡胶 | D. | 聚氯乙烯 |
7.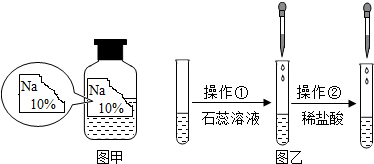 某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
【猜想与假设】溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如下:
【探究过程】如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是石蕊试液变成蓝色;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的氢氧化钠.
【探究结论】你认为该溶液中的溶质可能是上述假设物质中的碳酸钠,你的判断依据是碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以.
【探究反思】(1)若上述探究结论是正确的,操作②产生的气体应是CO2(写化学式),实验室检验该气体的实验操作及现象是将气体通入石灰水,石灰水变浑浊.
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述列表信息.请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由:若滴加石蕊试液变成蓝色,则不含有硫酸钠.
 某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.【猜想与假设】溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究结论】你认为该溶液中的溶质可能是上述假设物质中的碳酸钠,你的判断依据是碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以.
【探究反思】(1)若上述探究结论是正确的,操作②产生的气体应是CO2(写化学式),实验室检验该气体的实验操作及现象是将气体通入石灰水,石灰水变浑浊.
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述列表信息.请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由:若滴加石蕊试液变成蓝色,则不含有硫酸钠.
11.在一定温度下,向100g水中分别加入了质量分数为98%的浓硫酸、氧化钠、硫酸铜晶体(CuSO4•5H20)、碳酸钠各5g,充分搅拌形成溶液.
①实验2和实验3形成的溶液混合后观察到的现象是有蓝色沉淀生成
②实验1和实验4形成的溶液混合、充分反应后,滴加石蕊试液,石蕊试液显示的颜色为红色(通过分析计算说明,写出计算过程).
| 实验序号 | 实验1 | 实验2 | 实验3 | 实验4 |
| 水的质量 | 100g | 100g | 100g | 100g |
| 加入物质质量 | 98%的浓硫酸5g | 氧化钠5g | 硫酸铜晶体5g | 碳酸钠5g |
②实验1和实验4形成的溶液混合、充分反应后,滴加石蕊试液,石蕊试液显示的颜色为红色(通过分析计算说明,写出计算过程).
12.下列洗涤方法中涉及到乳化作用的是( )
| A. | 用氢氧化钠溶液清洗盛装过植物油的瓶子 | |
| B. | 用酒精或汽油清洗掉衣服上的油污 | |
| C. | 用稀盐酸清洗盛装过石灰水的试剂瓶 | |
| D. | 加了餐具洗洁精的热水洗涤碗碟上的油污 |





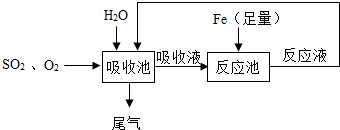 某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.
某研究人员按如图所示流程进行“燃煤烟气的脱硫研究”.实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环.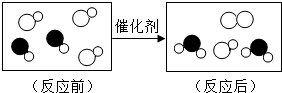 化学与生活、生产密切相关,请用所学的知识下列填空
化学与生活、生产密切相关,请用所学的知识下列填空