题目内容
8. 化学与生活、生产密切相关,请用所学的知识下列填空
化学与生活、生产密切相关,请用所学的知识下列填空①现有四种常见物质:H2SO4、CO2、Ca(OH)2、Na2CO3,其中属于氧化物的是CO2,属于酸的是H2SO4,焰色反应呈黄色的是Na2CO3,其水溶液呈碱性的是Ca(OH)2、Na2CO3.
②水在通电条件下反应的化学方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,生成氢气和氧气的体积比是2:1,0.5mol水中约含6.02×1023个氢原子(用科学计数法表示).
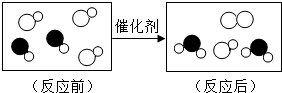
③下图是将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.
正确的说法是D.
A.该反应是置换反应
B.该反应中生成物的元素形态都为化合态
C.此化学反应有三种新物质生成
D.参加反应的两种分子的个数比为1:1.
分析 ①根据氧化物是指含有两种元素其中一种是氧元素的化合物;酸是指电离出的阳离子全部是氢离子的化合物;进行解答.
②首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
③根据变化微观示意图及粒子构成模拟图,可判断该变化为两种化合物的分子通过原子的重新结合生成一种单质分子和一种化合物分子,反应前后有一个构成相同的分子,可判断该分子未参加反应,因此该反应为两种不同的分子各2个参加反应,生成一种同种原子构成的单质分子1个和一种不同种原子构成的化合物分子2个.
解答 解:①氧化物是指含有两种元素其中一种是氧元素的化合物,所以属于氧化物的是二氧化碳;酸是指电离出的阳离子全部是氢离子的化合物,所以属于酸的是硫酸;焰色反应火焰呈黄色的是碳酸钠;其水溶液呈碱性的是氢氧化钙和碳酸钠.
②水通电分解生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.生成氢气和氧气的体积比是2:1,0.5mol水中约含1mol氢原子,即6.02×1023个氢原子;
③A、反应前的分子全部为不同种原子构成的化合物的分子,反应物中没有单质参加反应,因此该反应不属于置换反应;故错误;
B、该反应中生成物的元素形态一种为化合态,一种为游离态;故错误;
C、反应为两种不同的分子各2个参加反应,生成一种同单质分子和一种化合物分子,生成物有两种物质;故错误;
D、反应前的两种分子各有2个分子参加反应,因此参加反应的两种分子的个数比为1:1;故正确;
故填:①CO2;H2SO4;Na2CO3;Ca(OH)2、Na2CO3;②2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;2:1 6.02×1023 ③D.
点评 应熟悉生活中常见物质的成分,然后利用组成和元素来判断物质的类别,学会书写化学方程式,理由图示分析各微粒的个数比.

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案| A. | 水是由氢原子和氧原子构成的 | |
| B. | 水由液态变成气态时水分子质量变小 | |
| C. | 保持水的化学性质的微粒是水分子 | |
| D. | 水结冰后体积变大是水分子的体积增大造成的 |
| A. | 生石灰 | B. | 碳酸钙粉末 | C. | 氢氧化钙溶液 | D. | 氢氧化钠溶液 |
| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素中碳元素的含量最高 | |
| C. | 青蒿素中碳、氢和氧三种元素的质量比为15:22:25 | |
| D. | 青蒿素由15个碳原子、5个氧原子和22个氢原子构成 |
| A. | 在超低温世界里,钛会变得更为坚硬,并有超导体的性能 | |
| B. | “钛飞机”坚实又轻便,一架大型钛客机可比同样重的普通飞机多载100余人 | |
| C. | 钛金属外观似钢,具有银灰光泽 | |
| D. | 钛在高温下极易和空气发生反应 |

 A、B、C、D、E、F是初中化学中常见物质,它们的转化关系如图所示,(反应条件已略去).已知:B、C为黑色固体.
A、B、C、D、E、F是初中化学中常见物质,它们的转化关系如图所示,(反应条件已略去).已知:B、C为黑色固体.