题目内容
8.二氧化硫是大气的主要污染物,严禁直接排放,工业上常用NaOH溶液来吸收.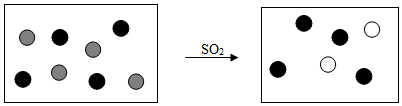
(1)写出NaOH溶液吸收SO2的化学方程式SO2+2NaOH═Na2SO3+H2O.
(2)图中小球分别表示NaOH溶液及吸收SO2后所得溶液中溶质的微粒,其中“●”表示的微粒是钠离子.
分析 (1)根据二氧化硫与氢氧化钠的反应写出反应的化学方程式;
(2)根据微粒的变化分析“●”表示的微粒.
解答 解:(1)NaOH溶液吸收SO2生成了亚硫酸钠和水,反应的化学方程式是:SO2+2NaOH═Na2SO3+H2O.
(2)由NaOH溶液吸收SO2的反应及溶液中微粒的变化可知,“●”在反应前后没有变化,应为钠离子.
故答为:(1)SO2+2NaOH═Na2SO3+H2O.(2)钠离子.
点评 了解二氧化硫和氢氧化钠的反应和溶液中微粒的变化是解答本题的基础知识.

练习册系列答案
相关题目
18.下列依据实验目的所设计的实验操作正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CaCl2溶液中的HCl | 加入过量的CaCO3后过滤 |
| B | 鉴别NaOH和Na2CO3 | 滴加酚酞试液 |
| C | 除去NaOH溶液中的Ca(OH)2 | 滴加过量的Na2CO3溶液后过滤 |
| D | 检验CO2气体 | 插入燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
19.下列有关溶液的说法中,错误的是( )
| A. | 外界条件不改变,溶质不会从溶液中分离出来 | |
| B. | 物质的溶解过程通常会伴随着能量的变化 | |
| C. | 溶液中的溶质以分子或离子的形式均匀分散在溶剂中保持静止不动,所以溶液具有均一性和稳定性 | |
| D. | 改变条件,能够使饱和溶液与不饱和溶液相互转化 |
3.如图是某化学反应的微观示意图,其中“ ”和“
”和“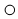 ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )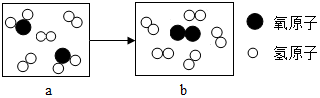
 ”和“
”和“ ”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
”分别表示两种质子数不同的原子,a、b分别表示反应前和反应后的物质,下列关于该反应前、后的说法不正确的是( )
| A. | 反应前后原子总数不变 | B. | a、b均为混合物 | ||
| C. | 该反应为分解反应 | D. | a中两种物质均为化合物 |
8.液氨可用作清洁燃料,其燃烧时的主要反应为4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2X+6H2O.下列有关说法中不正确的是( )
| A. | X的化学式为N2 | B. | 上述反应的类型属于置换反应 | ||
| C. | 液氨属于化合物 | D. | 反应前后氨元素的化合价降低 |
 2016年11月3日,我国大推力运载火箭长征五号发射成功,我国具备了建造空间站的能力.
2016年11月3日,我国大推力运载火箭长征五号发射成功,我国具备了建造空间站的能力.