题目内容
3.下列关于四种粒子的结构示意图的说法中正确的是( )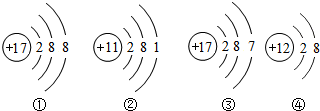
| A. | ①③是不同种元素 | |
| B. | ④属于离子,粒子符号为Mg-2 | |
| C. | ②③的化学性质相似 | |
| D. | ②表示的元素在化合物中通常显+1价 |
分析 A、元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),据此进行分析判断.
B、当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
C、元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似.
D、化合价的数值等于离子所带电荷的数值,且符号一致.
解答 解:A、元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),①③的质子数相同,属于同种元素,故选项说法错误.
B、④质子数=12,核外电子数=10,质子数>核外电子数,为带2个单位正电荷的镁离子,离子符号为Mg2+,故选项说法错误.
C、元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,②③的最外层电子数不同,它们的化学性质不相似,故选项说法错误.
D、②原子的最外层电子数为1,在化学反应中易失去1个电子而形成带1个单位正电荷的阳离子,化合价的数值等于离子所带电荷的数值,且符号一致,则该元素的化合价为+1价,故选项说法正确.
故选:D.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
3.下图所示的实验操作正确的是( )
| A. |  稀释浓硫酸 | B. | 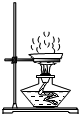 蒸发 | C. |  过滤 | D. | 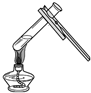 加热液体 |
20.下列物质的用途主要取决于其物理性质的是( )
| A. | 用稀盐酸除去铁制品表面的铁锈 | B. | 用一氧化碳冶炼金属 | ||
| C. | 用金属铜制作电路板 | D. | 用熟石灰改良酸性土壤 |
8.下列关于元素的说法中,正确的是( )
| A. | 同种元素的原子化学性质相同,但是质量可能不同 | |
| B. | 物质都是由元素组成的,只能通过不同种元素相互组合构成物质 | |
| C. | 元素的种类是由质子数和中子数共同决定的 | |
| D. | 人造元素是通过化学方法合成的 |
15.下列做法有益人体健康的是( )
| A. | 霉变的大米洗净后食用 | |
| B. | 大量使用防腐剂,延长食品保存期 | |
| C. | 利用甲醛水溶液浸泡水产品防腐 | |
| D. | 每天摄入一定量的蔬菜水果等含维生素较多的食物 |
12.实验室常用二氧化锰和浓盐酸共热制氯气(一种常温下呈黄绿色的气体,化学式:Cl2),反应的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;下列关于该实验的说法中正确的是( )
| A. | 从发生装置中通出的气体往往含有氯化氢气体杂质 | |
| B. | 该实验无明显现象 | |
| C. | 浓盐酸配制稀盐酸时,必须用托盘天平、量筒、烧杯和玻璃棒 | |
| D. | 该反应是复分解反应 |
13.饮用含甲醇的酒,可造成失明,甚至中毒死亡.如图是甲醇燃烧的微观示意图(未配平),下列有关说法或化学方程式错误的是( )


| A. | 工业酒精中往往含有甲醇,禁止用工业酒精配制饮料酒 | |
| B. | CH3OH+3O2$\frac{\underline{\;点燃\;}}{\;}$CO2+4H2O | |
| C. | 每个甲醇分子比每个乙醇分子少一个原子团“CH2” | |
| D. | 等质量的甲醇与甲烷分别在足量氧气中完全燃烧,甲醇消耗的氧气比甲烷少 |
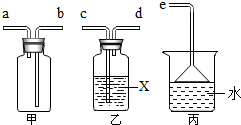 SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.
SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.