题目内容
2.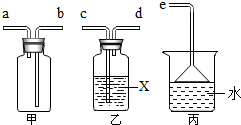 SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.
SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨.实验室用如图装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸,装置丙的作用吸收多余的二氧化硫气体,防止空气污染.
分析 二氧化硫的密度比空气大,因此应该从b进a出,干燥时应该c进d出,可以用浓硫酸干燥;二氧化硫易溶于水,排放到空气中会形成酸雨,因此用水吸收.
解答 解:二氧化硫应该先干燥,再收集,最后多余的用水吸收,防止污染.二氧化硫的密度比空气大,因此应该从b进a出,干燥时应该c进d出,可以用浓硫酸干燥;二氧化硫易溶于水,排放到空气中会形成酸雨,因此用水吸收.
故答案为:c→d→b→a;浓硫酸;吸收多余的二氧化硫气体,防止空气污染.
点评 本题属于常见气体的收集,收集较纯净的气体通常用排水法,能够考查学生的知识迁移运用能力.

练习册系列答案
相关题目
13.下列厨房常见物品放入水中能形成溶液的是( )
| A. | 花椒粉 | B. | 食盐 | C. | 面粉 | D. | 罗平菜籽油 |
17.实验室里有一瓶长期暴露在空气中的氢氧化钠固体,某化学兴趣小组对其进行了如下探究.
(1)确定固体的成分.
【提出猜想】猜想Ⅰ:固体中只含碳酸钠;
猜想Ⅱ:固体中只含氢氧化钠;
猜想Ⅲ:固体中含有碳酸钠和氢氧化钠.
【进行实验】
(2)测定固体中碳酸钠的质量分数.
【查阅资料】二氧化碳几乎不溶于饱和碳酸氢钠溶液中.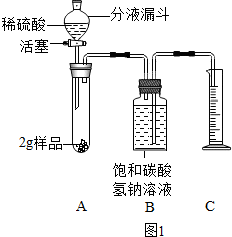
【进行实验】取2g固体,在25℃、101kPa下用图1所示装置进行实验,步骤如下:
①连接好装置并检查气密性;
②装入药品,通过分液漏斗滴加足量稀硫酸后,关闭分液漏斗活塞;
③充分反应后,恢复至25℃、101kPa,量筒中液体的体积为220mL.
【实验分析】
①装置B中的饱和碳酸氢钠溶液不能用水代替,原因是二氧化碳能够溶于水.
②充分反应后,装置A中残留的二氧化碳对实验结果是否有明显影响?没有(选填“有”或“没有”).
③已知在25℃、101kPa下二氧化碳的密度为1.8g/L,则固体中碳酸钠的质量分数为47.7%(结果保留至0.1%).
(3)除去固体中的碳酸钠.
【进行实验】实验流程如图2:
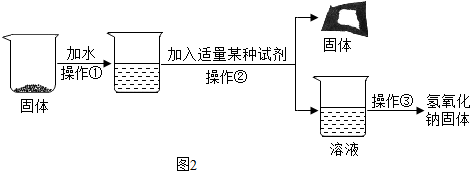
【实验分析】该流程中发生反应的化学方程式为Na2CO3+Ba(OH)2═BaCO3↓+2NaOH.操作①、②、③均需用到的一种仪器是玻璃棒.
(1)确定固体的成分.
【提出猜想】猜想Ⅰ:固体中只含碳酸钠;
猜想Ⅱ:固体中只含氢氧化钠;
猜想Ⅲ:固体中含有碳酸钠和氢氧化钠.
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量固体溶于水,加入 过量的氯化钡溶液; | 产生白色沉淀 | 猜想Ⅲ成立 |
| ②将上述反应后的混合液过滤,取少量滤液,加入无色酚酞试液. | 酚酞试液变红色 |
【查阅资料】二氧化碳几乎不溶于饱和碳酸氢钠溶液中.

【进行实验】取2g固体,在25℃、101kPa下用图1所示装置进行实验,步骤如下:
①连接好装置并检查气密性;
②装入药品,通过分液漏斗滴加足量稀硫酸后,关闭分液漏斗活塞;
③充分反应后,恢复至25℃、101kPa,量筒中液体的体积为220mL.
【实验分析】
①装置B中的饱和碳酸氢钠溶液不能用水代替,原因是二氧化碳能够溶于水.
②充分反应后,装置A中残留的二氧化碳对实验结果是否有明显影响?没有(选填“有”或“没有”).
③已知在25℃、101kPa下二氧化碳的密度为1.8g/L,则固体中碳酸钠的质量分数为47.7%(结果保留至0.1%).
(3)除去固体中的碳酸钠.
【进行实验】实验流程如图2:

【实验分析】该流程中发生反应的化学方程式为Na2CO3+Ba(OH)2═BaCO3↓+2NaOH.操作①、②、③均需用到的一种仪器是玻璃棒.
7.如图是初中化学中的一些重要实验.下列对如图所示实验的分析,不正确的是( )
| A. | 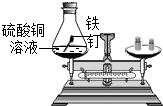 实验既可以说明铁能与硫酸铜反应,又可以验证质量守恒定律 | |
| B. | 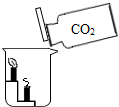 倾倒CO2时上层的蜡烛先熄灭,下层的蜡烛后熄灭 | |
| C. | 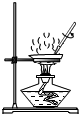 用玻璃棒搅拌的目的是防止局部受热造成液滴飞溅 | |
| D. | 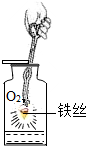 集气瓶内放少量水的目的是防止溅落的溶化物炸裂瓶底 |
14.一种以甲醇为原料的新型手机电池,能使手机的待机时间长达两个月,其反应原理为:2CH3OH+3X+4NaOH═2Na2CO3+6H2O,其中X的化学式、Na2CO3中碳元素的化合价分别是( )
| A. | CO2 +2 | B. | C O+2 | C. | H2 +4 | D. | O2 +4 |
3.下列关于四种粒子的结构示意图的说法中正确的是( )
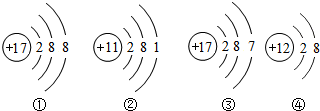

| A. | ①③是不同种元素 | |
| B. | ④属于离子,粒子符号为Mg-2 | |
| C. | ②③的化学性质相似 | |
| D. | ②表示的元素在化合物中通常显+1价 |
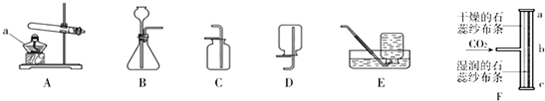
 在烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,向其中逐渐滴加质量分数为10%的稀HCl,放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答:
在烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,向其中逐渐滴加质量分数为10%的稀HCl,放出气体的质量与所滴入稀盐酸的质量关系曲线如图所示,请根据题意回答: