题目内容
13.某学习小组取某地石灰石样品25g进行测定实验,现将200g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),实验过程所得数据如下表.| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/g | 40 | 40 | 40 | 40 | 40 |
| 生成气体的总质量/g | 2.2 | m | 6.6 | 8.8 | 8.8 |
(1)m的值为4.4g.
(2)25g石灰石样品中碳酸钙的质量.
(3)反应完全后最终溶液中氯化钙的质量分数?(结果精确到0.1%)
分析 (1)根据分五次加入盐酸后,第一次生成2.2g二氧化碳,第四生成2.2g二氧化碳,说明第二次生成2.2g二氧化碳,所以m值是4.4g进行分析;
(2)根据最终生成二氧化碳质量是8.8g,求出碳酸钙的质量;
(3)根据碳酸钙和盐酸反应的化学方程式和生成二氧化碳的质量计算生成氯化钙的质量,然后计算出氯化钙的质量分数.
解答 解:(1)根据分五次加入盐酸后,第一次生成2.2g二氧化碳,第四生成2.2g二氧化碳,说明第二次生成2.2g二氧化碳,所以m值是4.4g,故填:4.4;
(2)设碳酸钙的质量为x,生成氯化钙的质量为y,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 8.8g
$\frac{100}{x}=\frac{44}{8.8g}$
x=20g
(3)$\frac{111}{44}=\frac{y}{8.8g}$
y=22.2g
所得溶液中氯化钙的质量分数为:$\frac{22.2g}{20g+200g-8.8g}×100%$=10.5%
答:25g石灰石样品中碳酸钙的质量为20g,反应完全后最终溶液中氯化钙的质量分数为10.5%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性.

练习册系列答案
相关题目
7.要除去下列物质中的少量杂质(括号内物质为杂质),下列实验方案设计中,不合理的是( )
| A. | N2(O2)-将气体通过灼热的铜网,充分反应 | |
| B. | 稀硝酸(稀硫酸)-加入适量硝酸钡溶液,过滤 | |
| C. | NaCl(Na2CO3)-加入适量的Ca(OH)2溶液、过滤 | |
| D. | 铜粉(铁粉)-加入过量硫酸铜溶液,过滤 |
4.下列化学用语与所表达的意义对应正确的是( )
| A. | 2N2--4个氮原子 | B. | 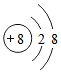 --氧原子 --氧原子 | ||
| C. | 2Fe2+--2个铁离子 | D. | Ag--金属银 |
5.下列各组物质按:名称(或俗名)、化学式、类别对应正确的一组是( )
| A. | 纯碱、NaOH、碱 | B. | 小苏打、NaHCO3、盐 | ||
| C. | 高锰酸钾、KMnO4、氧化物 | D. | 胆矾、CuSO4、盐 |
3.下列物质的俗名与化学式书写错误的是( )
| A. | 生石灰--CaO | B. | 熟石灰--Ca(OH)2 | C. | 纯碱--NaCO3 | D. | 烧碱--NaOH |
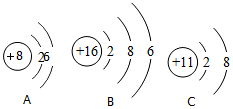 在宏观、微观和符号之间建立联系是化学学科特点
在宏观、微观和符号之间建立联系是化学学科特点
 人体缺少钙元素会影响健康,因此每日需摄入足够的钙.市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算
人体缺少钙元素会影响健康,因此每日需摄入足够的钙.市场上某钙制剂的说明书如图所示,请仔细阅读,并进行计算