题目内容
18.回答下列问题(1)氧气可压缩储存于钢瓶中,因为受压时氧气分子间的间隔减小;
(2)CH4充分燃烧可用化学方程式表示为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(3)炒菜时锅里的油不慎着火,可用锅盖盖灭,其灭火原理是隔绝氧气.
(4)净水过程中常用活性炭出去水中的色素.
分析 (1)构成物质的微粒具有如下特征:①体积和质量都很小②微粒之间存在间隔③微粒是在不断运动的,温度越高,分子运动越快.运用这些特征我们可以解释日常生活中的某些现象.
(2)根据甲烷在点燃条件下燃烧生成二氧化碳和水解答;
(3)根据灭火的原理解答;
(4)根据活性炭具有吸附性进行分析.
解答 解:(1)氧气可压缩储存于钢瓶中,因为受压时氧气分子间的间隔减小.
(2)甲烷在点燃条件下燃烧生成二氧化碳和水,反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)炒菜时锅里的油不慎着火,可用锅盖盖灭,其灭火原理是隔绝氧气.
(4)活性炭具有吸附性,净水过程中常用活性炭除去水中的色素.
故填:(1)间隔;(2)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;(3)隔绝氧气;(4)活性炭.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.考查学运用微粒的特征解释日常生活中的某些现象.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
11.水和溶液在生产、生活中起着十分重要的作用.请回答下列问题.
(1)不论是自来水还是纯净水,你认为保持水化学性质的最小粒子是水分子(写名称).
(2)下列做法不符合节约用水的是D
A.使用节水龙头
B.用淘米水洗碗
C.用喷灌、滴灌方法给农作物浇水
D.使用不间断地放水,边冲淋、边排水,用水量为165L/次的家用洗衣机
(3)一定浓度的溶液广泛用于工农业生产和实验室中.
①20℃时,将4.0g 硝酸钾固体放在一个小烧杯中,加36.0mL的水,配制得到溶液的溶质质量分数为10%(计算结果保留整数)
②称量硝酸钾固体时,分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
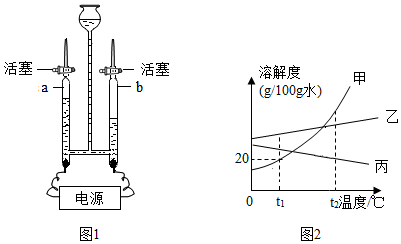
③量取所需蒸馏水要用到的仪器是BC(如图填字母).

④在20℃时,要将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从下表中找出需要用到的数据:1.063g/mL.
硝酸钾溶液的密度(单位lg/mL)
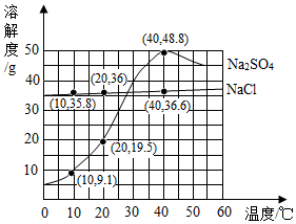
⑤如图为Na2SO4和NaCl的溶解度曲线. 下列叙述不正确的是BD.
A.将相同质量的Na2SO4和NaCl的饱和溶液从40℃降温至10℃,前者析出晶体的质量大
B.45℃时,使Na2SO4饱和溶液析出晶体的措施除加热升温、冷却降温和蒸发水3种方法外,还有其他方法
C.20℃时,向125g溶质质量分数为20%的食盐水中加入15g NaCl粉末并振荡,会出现浑浊
D.可用降温结晶法提纯含少量Na2SO4的NaCl.
(1)不论是自来水还是纯净水,你认为保持水化学性质的最小粒子是水分子(写名称).
(2)下列做法不符合节约用水的是D
A.使用节水龙头
B.用淘米水洗碗
C.用喷灌、滴灌方法给农作物浇水
D.使用不间断地放水,边冲淋、边排水,用水量为165L/次的家用洗衣机
(3)一定浓度的溶液广泛用于工农业生产和实验室中.
①20℃时,将4.0g 硝酸钾固体放在一个小烧杯中,加36.0mL的水,配制得到溶液的溶质质量分数为10%(计算结果保留整数)
②称量硝酸钾固体时,分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
③量取所需蒸馏水要用到的仪器是BC(如图填字母).

④在20℃时,要将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从下表中找出需要用到的数据:1.063g/mL.
硝酸钾溶液的密度(单位lg/mL)
| 温度 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |

⑤如图为Na2SO4和NaCl的溶解度曲线. 下列叙述不正确的是BD.
A.将相同质量的Na2SO4和NaCl的饱和溶液从40℃降温至10℃,前者析出晶体的质量大
B.45℃时,使Na2SO4饱和溶液析出晶体的措施除加热升温、冷却降温和蒸发水3种方法外,还有其他方法
C.20℃时,向125g溶质质量分数为20%的食盐水中加入15g NaCl粉末并振荡,会出现浑浊
D.可用降温结晶法提纯含少量Na2SO4的NaCl.
下列事实的解释不正确的是( )
事 实 | 解 释 | |
A | 氯化钠溶液能导电 | 溶液中有自由移动的电子 |
B | 双氧水能杀菌消毒而水不能 | 分子构成不同 |
C | 春天的揭西到处可以闻到花香 | 分子是不断运动的 |
D | 夏天钢轨间的缝隙变小 | 原子间间隔变大 |
A. A B. B C. C D. D
13.某学习小组取某地石灰石样品25g进行测定实验,现将200g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),实验过程所得数据如下表.
请计算:
(1)m的值为4.4g.
(2)25g石灰石样品中碳酸钙的质量.
(3)反应完全后最终溶液中氯化钙的质量分数?(结果精确到0.1%)
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/g | 40 | 40 | 40 | 40 | 40 |
| 生成气体的总质量/g | 2.2 | m | 6.6 | 8.8 | 8.8 |
(1)m的值为4.4g.
(2)25g石灰石样品中碳酸钙的质量.
(3)反应完全后最终溶液中氯化钙的质量分数?(结果精确到0.1%)
10.下列物质的主要成分与化学式相符合的是( )
| A. | 纯碱 NaOH | B. | 天然气 CH4 | C. | 生石灰 Ca(OH)2 | D. | 苏打 NaHCO3 |
8.分析处理图表中的信息是学习化学的一种重要方法. 如表是氯化钠和硝酸钾在不同温度时的溶解度,仔细阅读并回答下列问题.
(1)上述两种物质中,NaCl(填化学式)的溶解度受温度影响较小.
(2)在40℃时,将40g硝酸钾固体加入到100g水中,搅拌充分后得到是不饱和溶液(填“饱和”或“不饱和”).
(3)针对上述信息,甲、乙、丙三位同学分别得到如下结论,你认为说法正确的是乙.
甲:KNO3饱和溶液中一定不能再溶解NaCl固体.
乙:KNO3与NaCl溶解度相等时的温度一定在20℃-40℃之间.
丙:40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大.
| 温度/℃ | 20 | 40 | 60 | 80 | |
| 溶解度/g | NaCl | 36.0 | 36.6 | 37.3 | 38.4 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | |
(2)在40℃时,将40g硝酸钾固体加入到100g水中,搅拌充分后得到是不饱和溶液(填“饱和”或“不饱和”).
(3)针对上述信息,甲、乙、丙三位同学分别得到如下结论,你认为说法正确的是乙.
甲:KNO3饱和溶液中一定不能再溶解NaCl固体.
乙:KNO3与NaCl溶解度相等时的温度一定在20℃-40℃之间.
丙:40℃时,KNO3溶液的溶质质量分数一定比NaCl溶液的溶质质量分数大.
 水在生活、生产和化学实验中起着十分重要的作用.
水在生活、生产和化学实验中起着十分重要的作用. 为将G20峰会办成零排放的绿色环保型会议,充分展示我国政府和社会各界推动低碳经济和可持续发展的信心与决心,在杭州临安市营造了334亩碳中和林,通过植树造林抵消会议的碳排放.
为将G20峰会办成零排放的绿色环保型会议,充分展示我国政府和社会各界推动低碳经济和可持续发展的信心与决心,在杭州临安市营造了334亩碳中和林,通过植树造林抵消会议的碳排放.