题目内容
10.请结合如图回答问题.
(1)利用甲装置进行实验的是:验证化学反应前后质量守恒,红磷在空气中燃烧的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实辁室利用乙装置制取并收集的某种气体,写出一个符合题意的制取该气体的化学方程式Zn+H2SO4=ZnSO4+H2↑.
(3)炭粉还原氧化铜的实轮装置如图丙所示,当看到澄清石灰水刚出现诨浊时,不能(填“能”或“不能”)确定氧化铜和炭粉已经开始反应,反应完全后,若仅撤走酒精灯停止加热,可能导致的后果是②中的液体通过导管流入①中,造成试管炸裂.
分析 (1)根据实验装置来分析其实验目的、根据化学方程式的书写方法来分析;
(2)根据制取装置与收集方法来分析;
(3)根据碳也可以与氧气反应生成二氧化碳以及实验的注意事项分析.
解答 解:(1)由甲装置可知,该实验是验证化学反应前后质量守恒;磷与氧气在点燃的条件下反应生成五氧化二磷;故填:验证化学反应前后质量守恒;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)乙中的制取装置适用于固液常温下反应,向下排空气法适用于收集密度比空气小的气体,则该装置可用于氢气的制取与收集;故填:Zn+H2SO4=ZnSO4+H2↑;
(3)当看到澄清的石灰水刚出现浑浊时,可能是炭与氧气反应生成的二氧化碳,故不能判断炭与氧化铜发生了反应;反应完全后,若仅撤走酒精灯停止加热,会造成试管内温度降低,压强减小,②中的液体通过导管流入①中,造成试管炸裂;故填:不能;②中的液体通过导管流入①中,造成试管炸裂.
点评 完成实验探究题时,要明确探究的目的,根据所给信息按步骤进行分析,认真思考反应中的现象,不放过细节问题.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
1.如图所示的四个图象,分别对应四种过程,其中不正确的是( )
| A. | 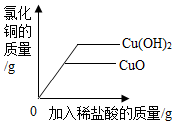 等质量的Cu(OH)2和CuO分别加入相同的稀盐酸 | |
| B. | 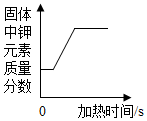 加热氯酸钾和二氧化锰的混合物制氧气 | |
| C. |  生石灰中加入一定质量的水 | |
| D. | 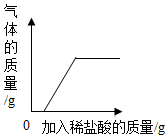 部分变质的氢氧化钠溶液中加入稀盐酸 |
2.“绿色发展”、“低碳生活”等理念逐渐深入民心,下列做法中,不符合这一理念的是( )
| A. | 使用废旧报纸制作铅笔杆 | B. | 生活中用火烧毁废旧塑料和橡胶 | ||
| C. | 发展快速公交,鼓励单车出行 | D. | 农业和园林改浸灌为喷灌和滴灌 |
19.下列说法正确的是( )
| A. | 生石灰和铁锈都是氧化物 | B. | 火碱和纯碱都是碱 | ||
| C. | 水银和银都是单质 | D. | 含碳元素的化合物一定是有机物 |
6.下列实验设计不能达到实验目的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 鉴别纯羊毛织品和涤纶织品 | 取样燃烧后闻气味 |
| B | 硬水软化 | 向硬水中加入肥皂水 |
| C | 鉴别一氧化碳和甲烷 | 点燃气体,在火焰上方罩干冷烧杯观察烧杯内壁是否出现液滴 |
| D | 验证在化学变化中分子可以再分 | 电解水实验,并检验生成的气体 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
13.某学习小组取某地石灰石样品25g进行测定实验,现将200g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),实验过程所得数据如下表.
请计算:
(1)m的值为4.4g.
(2)25g石灰石样品中碳酸钙的质量.
(3)反应完全后最终溶液中氯化钙的质量分数?(结果精确到0.1%)
| 次数 | 1 | 2 | 3 | 4 | 5 |
| 加入稀盐酸的质量/g | 40 | 40 | 40 | 40 | 40 |
| 生成气体的总质量/g | 2.2 | m | 6.6 | 8.8 | 8.8 |
(1)m的值为4.4g.
(2)25g石灰石样品中碳酸钙的质量.
(3)反应完全后最终溶液中氯化钙的质量分数?(结果精确到0.1%)
17.分离、除杂和检验是化学实验的重要环节,下列说法不正确的是( )
| A. | 分离CO2、CO混合物时,先用NaOH溶液吸收掉CO2,分离出CO,再向该溶液加足量稀盐酸“释放”出CO2 | |
| B. | 要除去CaCl2溶液中混有少量稀盐酸可加入过量的CaCO3充分反应后过滤 | |
| C. | 只用一种试剂无法把稀盐酸、BaCl2溶液和KNO3溶液三种溶液区分开 | |
| D. | 只用组内溶液相互混合的方法就能将KOH、Na2SO4、CuSO4、MgCl2鉴别出来 |
 已知A、B分别是硫酸溶液和氢氧化钡溶液中的一种,如图表示向A中逐滴加入B溶液后的pH变化曲线.请写出你从曲线中获得的信息.
已知A、B分别是硫酸溶液和氢氧化钡溶液中的一种,如图表示向A中逐滴加入B溶液后的pH变化曲线.请写出你从曲线中获得的信息.