题目内容
16.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案可行的是CA.木炭粉(CuO)--在空气中灼烧
B.KCl溶液(CaCl2)--通入过量的CO2气体,过滤
C. H2气体(HCl气体)--依次通过足量的NaOH溶液和浓硫酸
D.NaCl溶液(Na2CO3)--加入适量的氯化钙溶液,过滤.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、木炭粉在空气中灼烧生成二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、CO2气体不能与氯化钙溶液反应,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
C、HCl气体能与足量的NaOH溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再通过浓硫酸进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、Na2CO3能与适量的氯化钙溶液反应生成碳酸钙沉淀和氯化钠,再进行过滤,能除去杂质且没有引入新的杂质,符合除杂原则.
故答案为:C;氯化钙溶液.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
7.实验室欲制取少量Fe2(SO4)3溶液,下列四项中哪项为最佳选择( )
| A. | 过量Fe粉与稀H2SO4 反应 | B. | 过量Fe2O3与稀H2SO4反应 | ||
| C. | 过量稀H2SO4 与Fe粉反应 | D. | 过量稀H2SO4与Fe2O3反应 |
11.氧化汞受热分解生成汞和氧气的反应前后,发生改变的是( )
| A. | 分子种类 | B. | 原子种类 | C. | 元素种类 | D. | 原子数目 |
8.下列实验方案合理的是( )
| 选项 | 实验目的 | 所用试剂与方法 |
| A | 除去CO中的CO2 | 通过灼热的氧化铜 |
| B | 除去中CaO的CaCO3 | 加入足量水,过滤 |
| C | 除去FeCl2溶液中CuCl2 | 加入足量锌粉,过滤 |
| D | 除去NaCl固体中的泥沙 | 溶解、过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
4.对于实验现象,养成良好的观察习惯非常重要,如下现象描述错误的是( )
| A. | 在盛有锌粒的试管中滴入适量盐酸,锌粒表面有气泡冒出 | |
| B. | 在盛有石灰石的试管中滴入适量盐酸,石灰石表面有气泡冒出 | |
| C. | 在空气中点燃镁条,剧烈燃烧,发出耀眼的白光,生成黑色粉末 | |
| D. | 加热硫酸铜晶体,蓝色晶体逐渐变成白色粉末,且试管口有水滴出现 |


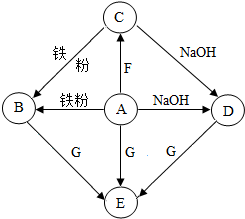 A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
