题目内容
7.要学会从化学的视角认识世界,对下列事实的解释不正确的是 ( )| 事 实 | 解 释 | |
| A | 走过花圃会闻到花香 | 分子不断地运动 |
| B | 金刚石很硬,而石墨较软 | 碳原子结构不同 |
| C | 湿衣服在夏天比冬天干的快 | 温度升高,分子能量增大,运动速率加快 |
| D | 冰水混合物属于纯净物 | 它们由同种分子构成 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,结合事实进行分析判断即可.
解答 解:A、闻到花香是因为分子在不断的运动,故选项解释正确.
B、金刚石硬而石墨软,是因为碳原子的排列方式不同,故选项解释错误.
C、分子是运动的,温度越高分子运动的速率越快,夏天在冬天温度高.所以,湿衣服在夏天比在冬天干的快.故选项解释正确.
D、冰水混合物是由水分子构成的,属于纯净物,故选项解释正确.
故选:B.
点评 本题难度不大,掌握分子的基本性质及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.吃馒头时,常常感觉到越嚼越甜.在这种变化中,起重要作用的是( )
| A. | 舌的搅拌 | B. | 牙齿的粉碎 | ||
| C. | 唾液中淀粉酶的催化 | D. | 水的润湿 |
18. CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
【查阅资料】
资料一:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列五种溶液的pH大小情况:
表中pH大小情况揭示出复分解反应的一条规律:较强酸发生类似反应可以生成较弱酸.下列反应中不符合该规律的是D(填字母)
A、H2SO4+Na2CO3=2NaCl+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
资料二:常见干燥剂有①五氧化二磷②无水氯化钙③碱石灰④生石灰⑤浓硫酸
【实验探究】
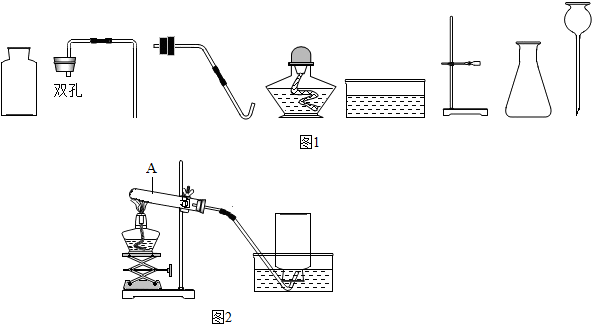
为了得到纯净的二氧化碳,设计了如图装置,请你分析:
a.制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
b.上述装置中,A是CuSO4溶液,B物质的名称可能是无水氯化钙(或五氧化二磷);
c.用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”).
 CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:
CaCO3广泛存在于自然界,是一种重要的化工原料.某种大理石除主要成分为CaCO3外,还有少量的硫化物.某同学用这种大理石和稀盐酸反应,开展以下探究:【查阅资料】
资料一:已知碳酸钙与盐酸的复分解反应可自发进行.在常温下,测得浓度均为a%的下列五种溶液的pH大小情况:
| 溶质 | H2SO4 | HCl | H2S | H2CO3 | HClO |
| pH | 小→大 | ||||
A、H2SO4+Na2CO3=2NaCl+2H2O+2CO2↑ B、2HCl+CaS=CaCl2+H2S↑
C、CO2+H2O+Ca(ClO)2=CaCO3↓+2HClO D、H2S+CuSO4=H2SO4+CuS↓
资料二:常见干燥剂有①五氧化二磷②无水氯化钙③碱石灰④生石灰⑤浓硫酸
【实验探究】
为了得到纯净的二氧化碳,设计了如图装置,请你分析:
a.制备的CO2气体中,可能含有的杂质是HCl、H2S、和水蒸气;
b.上述装置中,A是CuSO4溶液,B物质的名称可能是无水氯化钙(或五氧化二磷);
c.用这个实验得到的气体测定CO2的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”).
15.某同学用氯化钠固体和蒸馏水配制氯化钠溶液.他往95毫升水(密度为1g/cm3)中加入5克氯化钠固体,配制成了实验需要的溶液,把溶液全部装入试剂瓶后,贴上标签.该标签的书写正确的是( )
| A. |  | B. |  | C. |  | D. |  |
2.如图所示变化过程中发生物理变化的是( )
| A. |  蜡烛燃烧 | B. |  动植物的呼吸 | ||
| C. |  松花江水面结冰 | D. |  铜在潮湿的空气中生成铜绿 |
 2014年,黑龙江省的粮食产量又跃居全国第一,如图是某农场的一块麦田,请回答有关问题:
2014年,黑龙江省的粮食产量又跃居全国第一,如图是某农场的一块麦田,请回答有关问题: