题目内容
16.向某FeSO4和CuSO4的混合溶液中加入一定质量锌粉,充分反应后过滤,得滤液和滤渣.向滤渣中加入稀盐酸,有气泡产生.根据实验现象判断,下列说法中正确的是( )| A. | 滤液中一定存在Fe元素 | B. | 滤液的颜色呈蓝色 | ||
| C. | 滤渣中一定含有Fe和Cu | D. | 滤渣中可能还有铜粉 |
分析 在金属活动性顺序中,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把排在它后面的金属从其盐溶液中置换出来;锌的金属活动性比铁、铜强,锌与硫酸铜反应生成硫酸锌和铜,锌与FeSO4反应生成硫酸锌和铁;但当同一种金属置换比它弱的两种金属时,首先被置换出来的是金属活动性最弱的,当锌把硫酸铜中的铜完全置换出来,才能与硫酸亚铁溶液反应;向滤渣中加入稀盐酸,有气泡产生,说明滤渣中含有铁或铁、锌,据此进行分析判断.
解答 解:A、向滤渣中加入稀盐酸,有气泡产生,也可能是锌粉过量,若是这种情况,滤液中不存在Fe元素,故选项说法错误.
B、向滤渣中加入稀盐酸,有气泡产生,则说明固体中一定含有铁,或是铁和锌,说明锌已经把硫酸铜溶液完全反应,滤液的颜色不可能为蓝色,故选项说法错误.
C、向滤渣中加入稀盐酸,有气泡产生,则说明固体中一定含有铁,此时硫酸铜溶液中的铜离子早已被置换出来,则滤渣中一定含有Fe和Cu,故选项说法正确.
D、由C选项的分析,滤渣中一定含有铜,故选项说法错误.
故选:C.
点评 本题难度不大,考查金属活动性顺序并能灵活运用,掌握当同一种金属置换比它弱的两种金属时首先被置换出来的是金属活动性最弱的是正确解答本题的关键所在.

练习册系列答案
相关题目
6.pH=1的溶液中能大量共存并且溶液为无色透明的离子组是( )
| A. | Ba2+、Na+、NO3-、SO${\;}_{4}^{2-}$ | B. | Mg2+、Cl-、Al3+、SO${\;}_{4}^{2-}$ | ||
| C. | K+、Cl-、CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$ | D. | Ca2+、Na+、Fe3+、NO${\;}_{3}^{-}$ |
7.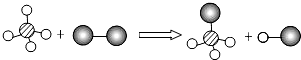 已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法中正确的是( )
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法中正确的是( )
 已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法中正确的是( )
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图:(说明:一种小球代表一种元素的原子)则下列说法中正确的是( )| A. | 该图示不符合质量守恒定律 | B. | 该反应属于置换反应 | ||
| C. | 图示中只有一种化合物 | D. | 图示中共有3种原子 |
4.由CaCl2、NaCl组成混合物,其中NaCl的质量分数为26%.将一定质量的混合物充分溶于水得到200g溶液,经测定溶液中钙元素的质量为2.4g,则该混合物中氯元素的质量为( )
| A. | 5.68g | B. | 2.84g | C. | 14.2g | D. | 0.71g |
11.铁在高温下能与水蒸气反应,生成四氧化三铁与氢气,该反应中还原剂是( )
| A. | 铁 | B. | 水 | C. | 四氧化三铁 | D. | 氢气 |
1.某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中没有氢元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
【交流与反思】由于过氧化钠常温下能与二氧化碳和水反应,所以保存过氧化钠一定要密封.
【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠 猜想b:碳酸氢钠
小周同学认为猜想b不成立,理由是反应物中没有氢元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸,产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2═2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量过氧化钠粉末于试管中,加入蒸馏水,再用带火星的木条伸入试管中 | 产生气泡 和带火星的木条复燃 | 过氧化钠能与水反应生成氧气 |
| ②向上述反应后的试管中滴加酚酞试液 | 溶液变红 | 所得溶液呈碱性,推断过氧化钠与 水反应生成NaOH(填化学式) |
6.某兴趣小组同学在实验室将一定量的稀硫酸加入到盛有氢氧化钠溶液的烧杯中,未看到明显的现象,部分同学产生疑问:酸和碱到底能否发生反应?
(1)该小组同学又做出了如下实验:
(2)同学们对(1)实验后溶液中的溶质组成展开探究,做出如下猜想:
小明的猜想是:只有Na2SO4;
小亮的猜想是:有Na2SO4和NaOH;
小丽的猜想是:有Na2SO4和H2SO4;
你认为小亮的猜想不合理.
若要验证余下两种猜想中的一种是正确的,请完成下面的实验方案.
(1)该小组同学又做出了如下实验:
| 实验步骤 | 实验现象 | 实验结论及反应方程式 |
| 向滴有酚酞溶液的稀氢氧化钠溶液的试管中,加入稀硫酸,并振荡 | 观察到溶液由红色变为无色 | 氢氧化钠和硫酸发生了反应,反应的化学方程式为H2SO4+2NaOH═Na2SO4+2H2O |
小明的猜想是:只有Na2SO4;
小亮的猜想是:有Na2SO4和NaOH;
小丽的猜想是:有Na2SO4和H2SO4;
你认为小亮的猜想不合理.
若要验证余下两种猜想中的一种是正确的,请完成下面的实验方案.
| 实验步骤 | 预期实验现象 | 实验结论 |
| 取(1)实验后溶液少量于试管中,加入锌粒 | 有气泡产生 (或没有气泡产生) | 小丽 (或小明)的猜想正确 |
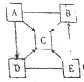 A~E是五种初中化学中常见的物质,它们之间的转化关系如图所示(图中“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能相互转化).其中A、B是黑色固体,C、D、E是无色气体,且B中含有世界年产量最高的金属.请回答下列问题:
A~E是五种初中化学中常见的物质,它们之间的转化关系如图所示(图中“-”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能相互转化).其中A、B是黑色固体,C、D、E是无色气体,且B中含有世界年产量最高的金属.请回答下列问题: