题目内容
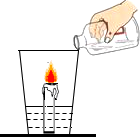 伶玲同学在家做实验(如图所示),杯底放一支小蜡烛和碳酸钠粉末,沿杯壁缓缓倒入一定量的醋(含有3%一5%的醋酸).他能观察到的现象有:
伶玲同学在家做实验(如图所示),杯底放一支小蜡烛和碳酸钠粉末,沿杯壁缓缓倒入一定量的醋(含有3%一5%的醋酸).他能观察到的现象有:(1)
(2)
考点:盐的化学性质,二氧化碳的化学性质
专题:实验性简答题
分析:(1)根据纯碱和醋酸的化学性质分析即可,纯碱的化学式是Na2CO3,醋酸的化学式是CH3COOH,两者可以反应生成二氧化碳气体,即Na2CO3+2CH3COOH═2CH3COONa+H2O+CO2↑;
(2)根据二氧化碳的物理化学性质分析即可,二氧化碳有密度比空气大,不燃烧也不支持燃烧的性质.
(2)根据二氧化碳的物理化学性质分析即可,二氧化碳有密度比空气大,不燃烧也不支持燃烧的性质.
解答:解:(1)因为醋酸和纯碱可以反应生成二氧化碳气体,所以首先看到有大量气泡产生;
(2)因为二氧化碳密度比空气大,所以生成的二氧化碳并未跑出玻璃杯,而是在玻璃杯底部,所以燃着的蜡烛熄灭.
故答案为:(1)溶液中有大量气泡生成;
(2)蜡烛逐渐熄灭.
(2)因为二氧化碳密度比空气大,所以生成的二氧化碳并未跑出玻璃杯,而是在玻璃杯底部,所以燃着的蜡烛熄灭.
故答案为:(1)溶液中有大量气泡生成;
(2)蜡烛逐渐熄灭.
点评:本题难度不大,掌握二氧化碳的物理性质、化学性质及碳酸盐的性质等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列能除去密闭容器中空气里的氧气而不引进其它气体杂质的是( )
| A、红磷 | B、硫磺 | C、蜡烛 | D、木炭 |
下列判断正确的是( )
| A、将100mL酒精与100mL水混合,能形成200mL溶液 |
| B、向饱和的硝酸钾溶液中加入5g硝酸钾固体,升温,硝酸钾固体质量增加 |
| C、a g氯酸钾与b g二氧化锰充分反应得到c g氧气,残留固体质量为d g,则d=a-c |
| D、向10 g溶质质量分数为10%的NaCl溶液中加入1 g水后,溶液中溶质的质量为1g |
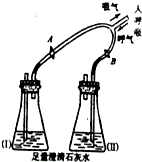 人体通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气.但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用了如图所示装置进行实验.
人体通过肺与外界进行气体交换,吸入空气中的氧气,排出二氧化碳和水蒸气.但人体排出的二氧化碳究竟是空气中原有的,还是人体代谢的最终产物?为了证实这个问题,有人采用了如图所示装置进行实验.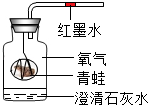 (1)现有空气、氧气、二氧化碳三种无色气体,请你从中任选二种气体,并用两种不同的方法鉴别它们.
(1)现有空气、氧气、二氧化碳三种无色气体,请你从中任选二种气体,并用两种不同的方法鉴别它们.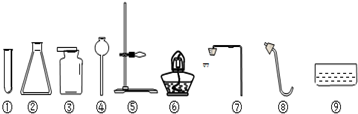
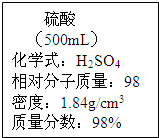 实验室一瓶浓硫酸的商标如图所示,根据有关信息计算.
实验室一瓶浓硫酸的商标如图所示,根据有关信息计算.