题目内容
下列判断正确的是( )
| A、将100mL酒精与100mL水混合,能形成200mL溶液 |
| B、向饱和的硝酸钾溶液中加入5g硝酸钾固体,升温,硝酸钾固体质量增加 |
| C、a g氯酸钾与b g二氧化锰充分反应得到c g氧气,残留固体质量为d g,则d=a-c |
| D、向10 g溶质质量分数为10%的NaCl溶液中加入1 g水后,溶液中溶质的质量为1g |
考点:分子的定义与分子的特性,饱和溶液和不饱和溶液相互转变的方法,用水稀释改变浓度的方法,质量守恒定律及其应用
专题:物质的微观构成与物质的宏观组成,化学用语和质量守恒定律,溶液、浊液与溶解度
分析:A.根据分子的特征来分析;B.根据硝酸钾的溶解度受温度的影响来分析;C.根据质量守恒定律来分析;D.溶液加水稀释过程中溶质的质量不变.
解答:解:A.因为分子间存在着间隔,故混合后的体积应小于200mL,故错误;
B.硝酸钾的溶解度随温度的升高而增大,故升温后,硝酸钾固体质量减少故错误;
C.根据质量守恒定律可知,a+b-c=d,故错误;
D.溶液加水稀释过程中,溶质的质量不变,故正确.
故选D.
B.硝酸钾的溶解度随温度的升高而增大,故升温后,硝酸钾固体质量减少故错误;
C.根据质量守恒定律可知,a+b-c=d,故错误;
D.溶液加水稀释过程中,溶质的质量不变,故正确.
故选D.
点评:本题考查的知识点较多,但是难度不大,需要加强基础知识的训练.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述正确的是( )
| A、门捷列夫发现元素周期律和元素周期表奠定了近代化学的基础 |
| B、绿色化学的核心就是要利用化学原理从源头消除污染 |
| C、化学研究的是自然界已存在的物质及其变化 |
| D、化学的发展必然导致生态环境的恶化 |
下列物质中含有氧气的是( )
| A、双氧水 | B、空气 |
| C、氯酸钾 | D、高锰酸钾 |
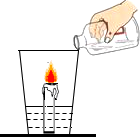 伶玲同学在家做实验(如图所示),杯底放一支小蜡烛和碳酸钠粉末,沿杯壁缓缓倒入一定量的醋(含有3%一5%的醋酸).他能观察到的现象有:
伶玲同学在家做实验(如图所示),杯底放一支小蜡烛和碳酸钠粉末,沿杯壁缓缓倒入一定量的醋(含有3%一5%的醋酸).他能观察到的现象有: