题目内容
10.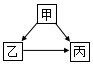 甲、乙、丙是初中化学中常见的三种物质,其中一种物质为单质,另外两种物质的组成元素相同,其转化关系如图所示.回答下列问题:
甲、乙、丙是初中化学中常见的三种物质,其中一种物质为单质,另外两种物质的组成元素相同,其转化关系如图所示.回答下列问题:(1)若丙为单质,则甲→丙的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,乙→丙的反应条件是通电;
(2)若甲为单质,则甲→乙的化学化学方程式为2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO,该反应属于化合反应(填分解或化合).
分析 要根据学过的知识进行有依据性的猜测,应熟记常见物质的性质和用途.
解答 解:
(1)若丙为单质,则可认为,甲是过氧化氢、乙是水,丙是氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,水通电能生成氧气,故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;通电;
(2)若甲为单质,则认为甲是碳,乙是一氧化碳,丙是二氧化碳,则碳和氧气点燃生成一氧化碳,属于化合反应,故填:2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO;化合.
点评 熟记常见物质的性质和用途;要根据学过的知识进行有依据性的猜测,应熟记常见物质的性质和用途.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
14.下列曲线正确的是( )
| A. |  向盐酸中加水 向盐酸中加水 | B. |  浓H2SO4加入水中 浓H2SO4加入水中 | ||
| C. |  煅烧CaCO3 煅烧CaCO3 | D. |  O2 在水中的溶解性 |
1.某学生用一种不纯的锌粒和稀硫酸反应,共做了五组对比实验,实验结果记录如下:
(1)上表中m=6.44g、n=10.80g;
(2)上述五组实验中,反应后硫酸有剩余的是1、2、3(填组序号);
(3)计算所用锌粒的纯度.
(4)计算稀硫酸的质量分数.
| 实验序号 | 加入锌的质量/g | 稀硫酸的体积/mL | 生成硫酸锌的质量/g |
| 1 | 1.5 | 40.O | 3.22 |
| 2 | 3.0 | 40.O | m |
| 3 | 4.5 | 40.O | 9.66 |
| 4 | 6.0 | 40.O | 10.80 |
| 5 | 7.5 | 40.O | n |
(2)上述五组实验中,反应后硫酸有剩余的是1、2、3(填组序号);
(3)计算所用锌粒的纯度.
(4)计算稀硫酸的质量分数.
5.日常生活中的下列做法,不正确的是( )
| A. | 用煤炉取暖,可在煤炉上放一壶水以防煤气中毒 | |
| B. | 进入气体不畅通的枯井前,先用蜡烛做灯火实验 | |
| C. | 用食醋除去热水瓶胆内的水垢 | |
| D. | 用干冰制造出舞台上云雾缭绕的景象 |
15.有两包黑色粉末,一包是铁粉,一包是氧化铜粉末,能快速将二者鉴别出来的方法是( )
| A. | 在空气中加热 | B. | 测定密度 | C. | 与氢气反应 | D. | 用磁铁吸引 |
2.把铁片分别插入下列溶液中,一段时间后把铁片取出,溶液质量减少的是( )
| A. | 氯化镁溶液 | B. | 硫酸铜溶液 | C. | 盐酸 | D. | 硫酸亚铁溶液 |
 现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系:
现有A、B、C、D、E、F、G七种物质,C、F是最常见的金属,B是气体单质,D为浅绿色溶液,G为蓝色溶液,它们之间存在如图关系:
