题目内容
2.把铁片分别插入下列溶液中,一段时间后把铁片取出,溶液质量减少的是( )| A. | 氯化镁溶液 | B. | 硫酸铜溶液 | C. | 盐酸 | D. | 硫酸亚铁溶液 |
分析 根据在金属活动性顺序中,氢前的金属能与酸反应生成氢气,使溶液的质量增加,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,溶液质量的改变取决于参加反应的金属和生成的金属的质量差进行分析.
解答 解:A、在金属活动性顺序中,铁排在镁之后,所以把铁片放入氯化镁溶液中,不会反应,一段时间后,溶液质量不变,不符合题意,故A错误;
B、铁和硫酸铜反应生成硫酸亚铁和铜,每56份质量的铁可以置换出64质量的铜,反应后溶液质量减小,符号题意,故B正确;
C、铁和盐酸反应生成氯化亚铁和氢气,每56份质量的铁可以置换出2份质量的氢气,反应后溶液质量增加,不符合题意,故C错误;
D、铁和硫酸亚铁不会反应,反应后溶液质量不变,不符合题意,故D错误.
故选:B.
点评 本题考查了金属与酸和与盐溶液的反应,解答是可以依据反应前后的质量差进行分析,能较好考查学生分析、解决问题的能力.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
13.小林查阅资料获得有关物质燃烧的新信息:
(1)2Na+C12$\frac{\underline{\;点燃\;}}{\;}$2NaCl
(2)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.由此形成以下几点认识.
①反应(1)属于化合反应
②反应(2)属于分解反应
③燃烧不一定要有氧气参与
④使用CO2灭火应有所选择
其中正确的是( )
(1)2Na+C12$\frac{\underline{\;点燃\;}}{\;}$2NaCl
(2)2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C.由此形成以下几点认识.
①反应(1)属于化合反应
②反应(2)属于分解反应
③燃烧不一定要有氧气参与
④使用CO2灭火应有所选择
其中正确的是( )
| A. | 只有①②④ | B. | 只有①④ | C. | 只有①③④ | D. | 只有②⑨ |
17.下列各组物质间能发生反应的是( )
| A. | 铜与硫酸锌溶液 | B. | 银与稀硫酸 | C. | 锌与氯化钠溶液 | D. | 铝与硫酸铜溶液 |
11.下列物质不能由金属和稀硫酸反应直接制得的是( )
| A. | 硫酸铝 | B. | 硫酸铁 | C. | 硫酸锌 | D. | 硫酸镁 |
12.实现下列变化后,溶液的PH值变小的是( )
| A. | 蒸发海水析出食盐 | B. | 稀硫酸跟铁片反应 | ||
| C. | 向氢氧化钡溶液中通入二氧化碳 | D. | 向硫酸钠溶液中加入氢氧化钡 |
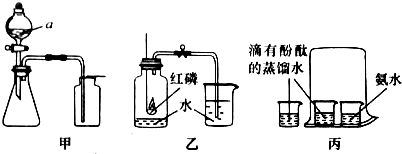
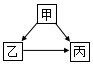 甲、乙、丙是初中化学中常见的三种物质,其中一种物质为单质,另外两种物质的组成元素相同,其转化关系如图所示.回答下列问题:
甲、乙、丙是初中化学中常见的三种物质,其中一种物质为单质,另外两种物质的组成元素相同,其转化关系如图所示.回答下列问题: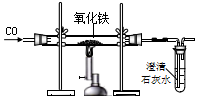 炼铁的原理是在高温条件下用一氧化碳还原铁的氧化物,在实验室里,小军同学利用如图所示的装置进行实验,请回答下列问题.
炼铁的原理是在高温条件下用一氧化碳还原铁的氧化物,在实验室里,小军同学利用如图所示的装置进行实验,请回答下列问题.