题目内容
3.请根据如图两个实验回答问题:
(1)A实验说明二氧化碳具有哪些性质(写出一点即可)?
(2)为什么用B实验无法验证质量守恒定律?
分析 (1)根据A实验的实验现象为蜡烛由低到高依次熄灭,澄清的石灰水变浑浊,进行分析解答.
(2)根据碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,生成的二氧化碳逸散到空气中,进行分析解答.
解答 解:(1)A实验会观察到蜡烛由低到高依次熄灭,蜡烛由低到高依次熄灭,说明了说明密度比空气的大;蜡烛熄灭,说明了CO2不能燃烧,也不支持燃烧;观察到澄清的石灰水变浑浊,说明了二氧化碳能与石灰水反应,两者反应生成碳酸钙沉淀和水.
(2)碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳,生成的二氧化碳逸散到空气中,故用B实验无法验证质量守恒定律.
故答案为:(1)密度比空气的大或不能燃烧也不支持燃烧或能与石灰水反应;(2)未在密闭的容器内进行,反应生成的CO2气体逸散到空气中.
点评 本题难度不大,熟练掌握二氧化碳的化学性质与物理性质、在设计验证质量守恒定律的实验时最好在密闭容器中进行是正确解答本题的关键.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
13.下列物质按照单质、氧化物、混合物的顺序排列的是( )
| A. | 铁、氧化铁、氯化铁 | B. | 冰、干冰、可燃冰 | ||
| C. | 金刚石、二氧化碳、铁锈 | D. | 氧气、铁矿石、石灰石 |

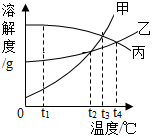 甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题: