题目内容
18.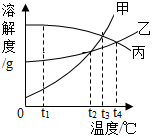 甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请据图回答下列问题:①t2℃时,甲和乙两种物质的溶解度相等.
②t3℃时,将甲、乙、丙的饱和溶液分别降温到t2℃时丙(选填“甲”、“乙”或“丙”)变为不饱和溶液.
③t1℃时,甲、乙、丙三种饱和溶液的溶质的质量分数由大到小的顺序为丙>乙>甲.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:①通过分析溶解度曲线可知,t2℃时,甲和乙两种物质的溶解度相等;
②丙物质的溶解度随温度的降低而增大,所以t3℃时,将甲、乙、丙的饱和溶液分别降温到t2℃时丙变为不饱和溶液;
③t1℃时,丙物质的溶解度最大,乙次之,甲物质的溶解对最小,所以甲、乙、丙三种饱和溶液的溶质的质量分数由大到小的顺序为:丙>乙>甲.
①t2;
②丙;
③丙>乙>甲.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
8.甲、乙、丙三位同学整理实验台时,发现一瓶氢氧化钠溶液没盖瓶塞,他们认为该溶液已经质变,变质原因用化学方程式表示为2NaOH+CO2═Na2CO3+H2O.
为进一步探究该溶液是否变质和变质程度,请你一起参与合作完成下列内容:
活动探究一:氢氧化钠溶液是否变质.
【实验过程】
三位同学把各自试管中的物质全部回收到一只大烧杯中.
(1)乙、丙同学一致认为甲同学实验不合理,理由是生成的碳酸钠溶液和剩余的氢氧化钠溶液都显碱性,都能使酚酞试液变红.
(2)一段时间后,同学们发现刚才盛放回收物的大烧杯中,杯底有白色沉淀,液体无色,此时大烧杯中的溶液,一定含有的溶质(酚酞除外)是NaCl,可能含有的溶质是CaCl2.
活动探究二:氢氧化钠溶液的变质程度.
【实验过程】
【反思】取完药液后要立即盖紧瓶塞.
为进一步探究该溶液是否变质和变质程度,请你一起参与合作完成下列内容:
活动探究一:氢氧化钠溶液是否变质.
【实验过程】
| 实验步骤 | 实验现象 | 实验结论 |
| 甲:取少量该溶液放入试管中,滴加几滴无色酚酞溶液 | 溶液变红 | 该溶液没有变质 |
| 乙:取少量该溶液放入试管中,加入一定量澄清石灰水 | 产生白色沉淀 | 该溶液已经变质,产生白色沉淀的化学方程式Na2CO3+Ca(OH)2═2NaOH+CaCO3↓ |
| 丙:取少量该溶液放入试管中,加入一定量稀盐酸 | 产生气泡 | 该溶液已经变质 |
(1)乙、丙同学一致认为甲同学实验不合理,理由是生成的碳酸钠溶液和剩余的氢氧化钠溶液都显碱性,都能使酚酞试液变红.
(2)一段时间后,同学们发现刚才盛放回收物的大烧杯中,杯底有白色沉淀,液体无色,此时大烧杯中的溶液,一定含有的溶质(酚酞除外)是NaCl,可能含有的溶质是CaCl2.
活动探究二:氢氧化钠溶液的变质程度.
【实验过程】
| 实验步骤 | 实验现象 | 结论 |
| 另取少量原溶液放入试管中,加入过量的CaCl2(BaCl2)溶液,振荡后再滴加酚酞试剂. | 产生白色沉淀,溶液由无色变为红色. | 该溶液已经部分变质 |
10.下列说法不符合客观事实的是( )
| A. | 生活中,氯化钠做融雪剂 | B. | 医疗上,碳酸钙做补钙剂 | ||
| C. | 工业上,纯碱用于制玻璃 | D. | 测pH时,将pH试纸浸入农夫山泉中 |


 归纳总结是学习化学的重要方法.小刚同学对碳及其重要化合物知识进行归纳、整理,并建构了如图所示的转化关系图.请回答下列问题
归纳总结是学习化学的重要方法.小刚同学对碳及其重要化合物知识进行归纳、整理,并建构了如图所示的转化关系图.请回答下列问题