题目内容
12. 元素周期表和原子结构示意图是学习和研究化学的重要工具.请根据以上示意图回答问题:
元素周期表和原子结构示意图是学习和研究化学的重要工具.请根据以上示意图回答问题:(1)根据A图可查出该原子的质子数是8,相对原子质量为16.00.
(2)B图中硫原子的质子数=中子数,则m值为32.
(3)C粒子的符号为Na+;该粒子的最外层电子数是8.
(4)A、B两种元素形成的氧化物有(填化学式)SO2、SO3.
分析 (1)根据元素周期表的信息来分析;
(2)根据相对原子质量≈质子数+中子数来分析;
(3)根据离子结构示意图以及离子符号的写法来分析;
(4)根据硫元素的化合物的种类来分析.
解答 解:(1)A图是氧元素元素周期表的信息,该原子的质子数为8,相对原子质量为16.00;故填:8;16.00;
(2)因为相对原子质量≈质子数+中子数,则硫原子的相对原子质量m=16+16=32;故填:32;
(3)C粒子核内有11个质子,核外电子数为10,是带有一个单位正电荷的钠离子,钠离子最外层有8个电子;故填:Na+;8;
(4)硫元素可以形成的氧化物主要有二氧化硫、三氧化硫;故填:SO2;SO3.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、离子结构示意图的含义是正确解答本题的关键.

练习册系列答案
相关题目
3.下列实验方案中,能达到实验目的是( )
| A. | 鉴别硬水和软水:加热煮沸或蒸馏 | |
| B. | 除去氧化铜中的碳粉:在密闭容器中加热 | |
| C. | 除去CO2中的CO:通入O2将CO点燃 | |
| D. | 区别KMnO4、FeSO4、CuSO4三种溶液:观察颜色 |
3.实验小组同学通过以下实验研究二氧化碳的性质.
(1)该实验可以说明分子具有的性质是分子是不断运动的.
(2)烧杯内壁上贴干的紫色石蕊纸条的目的是证明干燥的二氧化碳不能使紫色的石蕊试液变红色.
(3)该实验得出的结论是二氧化碳与水反应生成了碳酸.
(4)写出二氧化碳遇到石灰水发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
| 实验装置 | 实验操作 | 实验现象 |
 | ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的敞口集气瓶轻轻放入烧杯中 | 一段时间后,湿的紫色石蕊纸条变为红色 |
(2)烧杯内壁上贴干的紫色石蕊纸条的目的是证明干燥的二氧化碳不能使紫色的石蕊试液变红色.
(3)该实验得出的结论是二氧化碳与水反应生成了碳酸.
(4)写出二氧化碳遇到石灰水发生反应的化学方程式CO2+Ca(OH)2═CaCO3↓+H2O.
7.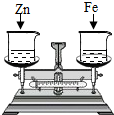 如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
 如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )
如图所示,天平调平后,在天平两盘的烧杯中各加入质量相等、质量分数相等足量的稀盐酸,同时向其中分别加入少量质量相等的锌片和铁片,则从反应开始到金属完全反应的过程中,天平指针指向的变化是( )| A. | 向左偏 | B. | 向右偏 | ||
| C. | 先向左偏后向右偏 | D. | 先向右偏后向左偏 |
17.如图一是氧、铝两种元素的原子结构示意图,图二是元素周期表的一部分,下列有关说法不正确的是( )


| A. | 图一只氧元素和铝元素在图二中的位置分别是⑤和⑦ | |
| B. | 钠元素和氯元素组成的物质是由离子构成的 | |
| C. | 氧原子在化学反应中容易得到两个电子变成阴离子,其符号为O2+ | |
| D. | 图二中①至⑨号元素中金属元素有3种 |
1.世界上物质多种多样,下列物质属于氧化物的是( )
| A. | 一氧化碳 | B. | 液氧 | C. | 氯酸钾 | D. | 稀盐酸 |
