题目内容
20. 同学们在实验室发现有一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分(如图)无法辨认具体是什么物质的溶液,只能看出溶质的质量分数为10%,经询问老师知道可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠溶液中的一种.为探究其成分,化学兴趣小组的同学进行如下探究,请你共同参与:
同学们在实验室发现有一瓶盛有无色溶液的试剂瓶,其标签破损,从残余部分(如图)无法辨认具体是什么物质的溶液,只能看出溶质的质量分数为10%,经询问老师知道可能是氢氧化钠、氯化钠、氢氧化钙或碳酸钠溶液中的一种.为探究其成分,化学兴趣小组的同学进行如下探究,请你共同参与:【查阅资料】小组同学查阅了相关资料,得知四种物质在常温下的溶解度如下表所示:
| 氢氧化钠 | 氯化钠 | 氢氧化钙 | 碳酸钠 | |
| 溶解度/g(20℃) | 51 | 36 | 0.16 | 21.5 |
【实验设计与探究】
(1)取少量样品溶液于试管中,往其中滴加酚酞试液,发现试液变红色,则该溶液不可能是氯化钠溶液.
(2)为了进一步确定该溶液的成分,兴趣小组的同学设计以下实验方案继续进行探究,请你帮忙完善实验操作及步骤.
| 实验操作及步骤 | 实验现象 | 实验结论 |
| 取少量样品溶液于试管中,滴加氯化钙溶液 | 有白色沉淀产生 | 该溶液是碳酸钠溶液 |
| 取少量样品溶液于试管中,滴加稀盐酸 | 有气泡产生 |
小组同学讨论后认为还可以通过往样品溶液中滴加澄清石灰水来确定该溶液的成分,请写出反应的化学方程式Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
分析 【讨论分析】氢氧化钙常温下的溶解度为0.18g,据此可计算出其饱和溶液的质量分数达不到10%,所以可判断不可能为氢氧化钙;
【实验设计与探究】氢氧化钠和碳酸钠的水溶液都是显碱性的溶液,都能够使酚酞试液变红色,氯化钠溶液显中性,不能使酚酞试液变色;
鉴别氢氧化钠和碳酸钠,可以用氯化钙溶液,能产生碳酸钙沉淀,也可以采用稀盐酸,能产生气体,两种方法都可以;
【实验反思】根据反应的原理写出反应的方程式.
解答 解:【讨论分析】常温下氢氧化钙的溶解度为0.18g,其饱和溶液中溶质质量分数=$\frac{0.18g}{0.18g+100g}$×100%<0.18%,而该溶液溶质质量分数为10%,所以不可能是氢氧化钙;故填:氢氧化钙;
【实验设计与探究】取少量样品于试管中,滴加酚酞试液,试液变红,说明该溶液可能是氢氧化钠溶液或碳酸钠溶液,该溶液不可能是氯化钠溶液;稀盐酸与碳酸钠反应产生二氧化碳气体;
故填:(1)氯化钠; (2)稀盐酸;
【实验反思】鉴别氢氧化钠和碳酸钠还可用澄清石灰水,能产生碳酸钙沉淀,方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
故填:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
点评 本题根据氢氧化钠、氯化钠、氢氧化钙、碳酸钠几种物质的性质特点,采取“利用测定结果进行先排除,最后进行实验检验的”方法确定未知溶液,涉及对四种物质相关性质及变化规律的考查.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
10.氢气是最理想的燃料,但目前还不能大规模的制取和利用,通过电解水的方法能制取氢气,但要消耗大量的电能.下列关于电解水的化学方程式2H2O$\frac{\underline{\;电解\;}}{\;}$ 2H2↑+02↑说法不正确的是( )
| A. | 水在通电的条件下生成氢气和氧气 | |
| B. | 分解的水的质量等于生成的氢气和氧气的质量和 | |
| C. | 每2个水分子分解生成2个氢分子和1个氧分子 | |
| D. | 每2g水分解生成2g氢气和1g氧气 |
11.传统“陈醋”生产过程中有一步称为“冬捞夏晒”,是指冬天捞出醋中的“冰”,夏日暴晒蒸发醋中的水分,以提高醋中的品质.假设用醋酸的质量分数为3%的半成醋,生产500g 5.4%的优级醋,过程中醋酸没有损失,捞出的冰和蒸发的水的总质量为( )
| A. | 500 g | B. | 100 g | C. | 200 g | D. | 400 g |
5.镍粉常用于各种高光泽装饰漆和塑料生产,也常用作催化剂.
I、【镍粉制备】:
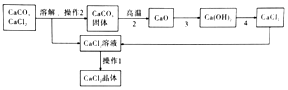
工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:

(1)反应器中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为CO2.
(2)物料在反应器中反应时需要控制反应条件.分析下图,反应器中最适合的温度及pH分别为55℃、8.3.
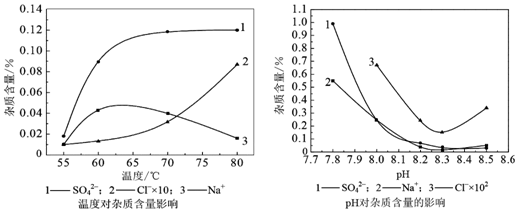
(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将升高(填“升高”、“降低”或“不变”).
(4)操作1的名称是过滤,实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒及漏斗,其中玻璃棒的作用是引流.
(5)固体洗涤时,需用纯水洗涤,检验其洗涤干净的试剂是BaCl2溶液或Ba(NO3)2溶液或Ba(OH)2溶液.
(6)气体Y是空气中含量最多的气体,其是氮气(填名称).
(7)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是便于快速晾干.
II、【测定碱式碳酸镍晶体的组成】:
为测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:
【资料卡片】:
1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.
2、400℃左右,NiO会氧化生成Ni2O3.
3、碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O.
【实验步骤】:
①检查装置气密性;②准确称取3.77g xNiCO3•yNi(OH)2•zH2O放在B装置中,连接仪器;③打开弹簧夹a,鼓入一段时间空气,称量装置C、D的质量;④关闭弹簧夹a,加热装置B至装置C中导管末端无气泡冒出;⑤打开弹簧夹a,缓缓通空气一段时间;⑥准确称量装置C、D的质量;⑦根据数据进行计算(相关数据如右表).
【实验分析及数据处理】:
(8)完善实验步骤中的填空:①检查装置气密性;⑤缓缓通空气一段时间.
(9)计算xNiCO3•yNi(OH)2•zH2O中x:y:z的值1:2:4.
(10)左侧通空气的目的是排尽装置中原有的CO2和水蒸气、将装置B中的CO2和水蒸气完全排出.
【实验反思】:
(11)实验结束后,称得装置B中残留固体质量为2.33g.请通过计算确定残留固体的组成及各成分的质量(2分,写出计算过程,精确到小数点后两位).剩余NiO质量为1.5g,生成Ni2O3 0.83g..
I、【镍粉制备】:
工业用电解镍新液(主要含NiSO4、NiCl2)制备碱式碳酸镍晶体xNiCO3•yNi(OH)2•zH2O,并利用其制备镍粉的流程如下:

(1)反应器中的一个重要反应为3NiSO4+3Na2CO3+2H2O=NiCO3•2Ni(OH)2+3Na2SO4+2X,X的化学式为CO2.
(2)物料在反应器中反应时需要控制反应条件.分析下图,反应器中最适合的温度及pH分别为55℃、8.3.

(3)生产中,pH逐渐增加,生成Ni(OH)2含量也相对增加,则生成的碱式碳酸镍晶体中,镍的含量将升高(填“升高”、“降低”或“不变”).
(4)操作1的名称是过滤,实验室完成此操作,需要的玻璃仪器是烧杯、玻璃棒及漏斗,其中玻璃棒的作用是引流.
(5)固体洗涤时,需用纯水洗涤,检验其洗涤干净的试剂是BaCl2溶液或Ba(NO3)2溶液或Ba(OH)2溶液.
(6)气体Y是空气中含量最多的气体,其是氮气(填名称).
(7)操作2含过滤、水洗、95%酒精浸泡、晾干等操作,其中用95%酒精浸泡的目的是便于快速晾干.
II、【测定碱式碳酸镍晶体的组成】:
为测定碱式碳酸镍晶体(xNiCO3•yNi(OH)2•zH2O)组成,某小组设计了如下实验方案及装置:

【资料卡片】:
1、碱式碳酸镍晶体受热会完全分解生成NiO、CO2及H2O.
2、400℃左右,NiO会氧化生成Ni2O3.
3、碱石灰是NaOH及CaO的混合物,可以吸收CO2和H2O.
【实验步骤】:
| 装置C/g | 装置D/g | 装置E/g | |
| 加热前 | 200.00 | 180.00 | 180.00 |
| 加热后 | 201.08 | 180.44 | 180.00 |
【实验分析及数据处理】:
(8)完善实验步骤中的填空:①检查装置气密性;⑤缓缓通空气一段时间.
(9)计算xNiCO3•yNi(OH)2•zH2O中x:y:z的值1:2:4.
(10)左侧通空气的目的是排尽装置中原有的CO2和水蒸气、将装置B中的CO2和水蒸气完全排出.
【实验反思】:
(11)实验结束后,称得装置B中残留固体质量为2.33g.请通过计算确定残留固体的组成及各成分的质量(2分,写出计算过程,精确到小数点后两位).剩余NiO质量为1.5g,生成Ni2O3 0.83g..
9.氦的元素符号是( )
| A. | H | B. | He | C. | Hg | D. | N |
10.下列化学方程式书写正确的是( )
| A. | 镁在空气中燃烧 Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 | |
| B. | 生石灰与水剧烈反应 CaO+H2O=Ca(OH)2 | |
| C. | 铁钉浸入硫酸铜溶液中 2Fe+3CuSO4=3Cu+Fe2(SO4) | |
| D. | 氢氧化钠溶液和硫酸铜溶液混合 CuSO4+NaOH=CuOH↓+NaSO4 |

 同学们学习了“氢氧化钠与盐酸的反应”后,都提出了以下问题:
同学们学习了“氢氧化钠与盐酸的反应”后,都提出了以下问题: