题目内容
15.合理运用燃烧与灭火的化学原理对保障生命财产安全非常重要.
(1)“燃烧的条件”实验中,把同样大小的滤纸碎片和乒乓球碎片分开放在一块薄铜片的两侧,加热铜片的中部,如图1所示,观察到的现象是乒乓球碎片先燃烧,通过此实验,说明燃烧的条件之一是温度需达到可燃物的着火点.
(2)据报导,某地发生火灾,有三名小孩生还.这三名小孩采取的措施是:一边用湿毛巾捂住嘴,一边低姿势前行.他们在逃生时主要利用了D(填字母).
A.湿毛巾可以供给水分
B.湿毛巾能吸收二氧化碳
C.低姿势前行是因为地面附近气压低
D.热空气密度小会上升,地面附近有毒气体相对较少
(3)如果某家庭用的是罐装液化石油气(主要成分是C3H8、C4H10、C3H6、C4H8),为了防止燃气泄漏造成危险,可以在厨房中安装泄气报警器(如图2所示).报警器的位置应按乙
(填“甲”或“乙”)图安装.
(4)在一密闭容器内有氧气、水蒸气、二氧化碳及一种未知物质M,在一定条件下充分反应,测得反应前后各物质的质量如表:(单位:g)
| 物质 | 氧气 | 二氧化碳 | 水蒸气 | M |
| 反应前质量 | 60 | 1 | 1 | 14 |
| 反应后质量 | 12 | 45 | 19 | x |
②已知未知物质M的相对分子质量为42,则该反应的化学方程式为2C3H6+9O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+6H2O.
(5)“绿色化学”的特点之一是“零排放”.一定条件下,一氧化碳和氢气可以按照不同比例反应,若只生成一种产物就能实现“零排放”,符合这一要求的产物可能是AC(填字母).
A.甲醇(CH3OH) B.乙醇(C2H5OH)
C.乙酸(CH3COOH) D.乙醛(CH3CHO)
分析 (1)可燃物燃烧需要同时具备两个条件:一是可燃物与氧气接触,二是温度要达到可燃物的着火点;
(2)热空气密度小而上升,地面附近有毒气体较少,并且在灭火或逃生过程中,湿毛巾可起到防毒面具的作用;
(3)可以根据燃气的性质分析;
(4)根据质量守恒定律以及化学方程式的写法来分析;
(5)根据“一氧化碳和氢气反应,只生成一种产物”可判断所生成的有机物中C、O元素的原子个数比应与CO中C、O元素的原子个数相同为1:1;根据所生成有机物中C、O元素的原子个数比,判断四个选项中符合此特点的化学式即该物质的化学式.
解答 解:(1)滤纸碎片和乒乓球碎片都与氧气接触,在加热过程中,由于乒乓球碎片的着火点较低,首先燃烧起来,说明燃烧需要温度达到可燃物的着火点.
故填:乒乓球碎片; 温度需达到可燃物的着火点;
(2)热空气密度小而上升,地面附近有毒气体较少,并且湿毛巾可起到防毒面具的作用,在灭火或逃生过程中,用湿毛巾捂住口鼻,能防止吸入烟尘中毒.
故选:D.
(3)因为罐装液化石油气的密度比空气大,所以报警器应该安装在比较低的地方.故填:乙;
(4)①由质量守恒定律可知,反应前后物质的总质量不变,所以60+1+1+14=12+45+19+x,则x=0;故填:0;
②该反应可表示为:M+O2→CO2+H2O,由质量守恒定律可知,M中一定含有碳元素与氢元素且与二氧化碳中的碳元素质量和水中氢元素的质量相同,则碳元素的质量为:(45g-1g)×$\frac{12}{44}×100%$=12g;氢元素的质量为:(19g-1g)×$\frac{1×2}{18}×100%$=2g;12g+2g=M的质量,则M中不含氧元素,设M的化学式为:CxHy,则$\frac{12x}{y}=\frac{12g}{2g}$,$\frac{x}{y}=\frac{1}{2}$,因为M的相对分子质量为42,所以M的化学式为C3H6.则反应的化学方程式为:2C3H6+9O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+6H2O;故填:2C3H6+9O2$\frac{\underline{\;点燃\;}}{\;}$6CO2+6H2O;
(5)A、根据化学式CH4O,可知该物质中C、O元素的原子个数比为1:1,符合所生成有机物的特点,故A正确
B、根据化学式C2H6O,可知该物质中C、O元素的原子个数比为2:1,不符合所生成有机物的特点,故B错误;
C、根据化学式CH3COOH,可知该物质中C、O元素的原子个数比为1:1,符合所生成有机物的特点,故C正确;
D、根据化学式C2H4O,可知该物质中C、O元素的原子个数比为2:1,不符合所生成有机物的特点,故D错误;
故选:AC.
点评 本题主要考查了燃气的性质及其爆炸、质量守恒定律及其应用等方面的知识,可以依据已有的课本知识进行.

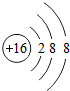 表示的粒子:S;④两个铁离子:2Fe3+;⑤地壳中含量最高的金属:Al;⑥+2价的镁元素:Mg2+.其中,正确的是( )
表示的粒子:S;④两个铁离子:2Fe3+;⑤地壳中含量最高的金属:Al;⑥+2价的镁元素:Mg2+.其中,正确的是( )| A. | ①④⑤ | B. | ②④⑤ | C. | ①③⑤ | D. | ①④⑥ |
| A. | -3 | B. | +1 | C. | +3 | D. | +5 |
| A. | 水是由氢气和氧气组成的 | |
| B. | 水电解后生成的氢气和氧气的体积比是2:1 | |
| C. | 用肥皂水可鉴别硬水与软水 | |
| D. | 工业污水应经过净化处理后在排放 |
| 序号 | A | B | C | D |
| 需区分的物质 | 生铁片和纯铁片 | 氯化钾和硫酸铵 | 氧化铁粉末和铜粉 | 氢氧化钙溶液和氯化钙溶液 |
| 第一方案 | 取样,分别加入足量的稀盐酸,观察是否有气泡产生 | 取样于研钵中,分别加入熟石灰,研磨,闻气味 | 分别取样,加入试管中,加入氢氧化钠溶液,观察现象 | 分别取样,加入试管中,测溶液的pH,比较数值 |
| 第二方案 | 取样,互相刻划,观察现象 | 取样,加入试管中,分别加入稀盐酸,观察现象 | 分别取样,放在白纸上,观察现象 | 分别取样,加入试管中,分别通入二氧化碳气体,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
| A | B | C | D |
 |  |  |  |
| 测定空气中氧气含量 | 铜与硝酸银溶液的反应 | 过滤 | 锌与稀盐酸的反应 |
(3)硝酸是一种具有氧化性的酸.已知铜与稀硝酸反应的化学方程式为:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,当硝酸的浓度增大,氧化性也增强,生成氮的氧化物中氮元素的化合价升高为+4价.请写出铜与浓硝酸反应的化学方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O.
