题目内容
10.已知在水溶液中,乙醇(C2H5OH)不发生电离,溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-).请回答下列问题:(1)根据溶液的组成推断,医用酒精(含乙醇75%的水溶液)显中性,溴化氢的水溶液显酸性(填“酸性”、“中性”或“碱性”);
(2)氢氧化钠的水溶液能导电而把氢氧化铜放入水中则不能导电的原因是氢氧化钠能溶于水,能解离出自由移动的钠离子和氢氧化根离子,氢氧化铜不溶于水,不能解离出自由移动的带电的微粒..
(3)氢氧化钠溶液中存在的微粒有(用化学符号表示)H2O、Na+、OH-.
分析 由于乙醇(C2H5OH)不发生电离,没有正负电荷的产生,不显电性,属于中性;溴化氢(HBr)电离产生氢离子(H+),属于酸;氢氧化铜不溶于水;氢氧化钠能溶于水,能解离出钠离子和氢氧根离子,还有构成水的水分子.据此分析回答有关的问题.
解答 解:(1)由于酒精在水溶液中不发生电离,在它的溶液中也就没有氢离子或者是氢氧根离子,所以酒精溶液既不显酸性也不显碱性;而溴化氢能发生电离产生氢离子,因此它的水溶液呈酸性;
故答案为:中性,酸性;
(2)由于氢氧化钠能溶于水,能解离出自由移动的钠离子和氢氧化根离子,氢氧化铜不溶于水,不能解离出自由移动的带电的微粒,所以,氢氧化钠的水溶液能导电而把氢氧化铜放入水中则不能导电;
(3)氢氧化钠溶液是氢氧化钠的水溶液,溶液中含有水分子、氢离子和氢氧化根离子,符号分别为:H2O、Na+、OH-.
故答案为:H2O、Na+、OH-.
点评 】本题难度不是很大,主要考查了有关酸的化学性质及中和反应的应用,培养学生的理解能力和分析能力.

练习册系列答案
相关题目
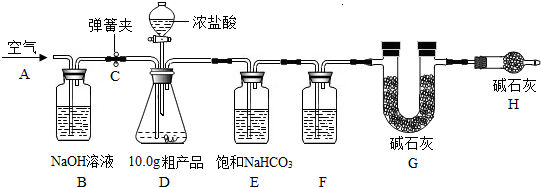
1.小羽同学用试管、长颈漏斗、量筒、水槽、胶塞(有孔)、玻璃导管、橡皮导管等器材设计出一套用碳酸钙与盐酸反应制取二氧化碳气体的实验装置.他用0.5克的碳酸钙与10克一定质量分数的盐酸反应,观察并用秒表记录产生二氧化碳气体所用的时间,实验记录如表.请你通过计算回答:
(1)反应的前2分钟内,每分钟平均产生二氧化碳气体的体积是55mL.若在当时的条件下(温度和压强不变),用10克碳酸钙与足量盐酸反应时,能产生0.12L二氧化碳气体.
(2)小羽同学在实验中发现,10克盐酸与0.5克的碳酸钙反应结束时盐酸只用去了一半的量,则原盐酸溶液中溶质的质量分数是多少?(列式计算)
| 时间(分钟) | 0.5 | 1 | 1.5 | 2 | 2.5 | 3 | 3.5 | 4 |
| 二氧化碳(mL) | 40 | 70 | 95 | 110 | 116 | 120 | 120 | 120 |
(2)小羽同学在实验中发现,10克盐酸与0.5克的碳酸钙反应结束时盐酸只用去了一半的量,则原盐酸溶液中溶质的质量分数是多少?(列式计算)
5.为了除去氯化钾中含有的少量硫酸镁和氯化钙杂质,需进行下列六项操作,先后次序正确的是( )
①加水溶解 ②加热蒸发得到晶体 ③加入过量的氯化钡溶液 ④加入适量的盐酸 ⑤加入过量碳酸钾和氢氧化钾 ⑥过滤.
①加水溶解 ②加热蒸发得到晶体 ③加入过量的氯化钡溶液 ④加入适量的盐酸 ⑤加入过量碳酸钾和氢氧化钾 ⑥过滤.
| A. | ①④③⑤⑥② | B. | ①⑤③④⑥② | C. | ①③④⑥⑤② | D. | ①③⑤⑥④② |
15.我国曾发生过多次将工业用盐如亚硝酸钠(NaNO2)误作食盐用于烹调而引起的中毒事件,关于亚硝酸钠的说法正确的是( )
| A. | 亚硝酸中钠、氧元素的质量比为23:32 | |
| B. | 亚硝酸钠中氧元素的质量分数最小 | |
| C. | 亚硝酸钠是氧化物 | |
| D. | 亚硝酸钠中氮元素化合价为+5价 |
2.对下列成语的有关化学原理解释合理的是( )
| 选项 | 成语 | 化学原理 |
| A | 釜底抽薪 | 燃烧需要可燃物 |
| B | 煽风点火 | 使温度达到可燃物的着火点 |
| C | 火上浇油 | 为燃烧提供足够多的氧气 |
| D | 钻木取火 | 燃烧需要达到着火点 |
20.正确的实验操作对实验结果、人身安全都非常重要.下列实验操作不正确的是( )
| A. |  滴加少量液体 | B. | 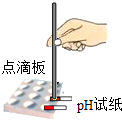 测定溶液pH | C. |  称量固体 | D. |  液体过滤 |