题目内容
20.回答下列有关检查装置的气密性的问题:
①热敷法(不能使用酒精灯加热装置)
操作:把装置连接好后,用双手捂住试管
现象:导管口有气泡冒出;
结论:装置气密性良好
②推拉法:缓慢拉活塞,玻璃管口有气泡冒出;缓慢推活塞玻璃管内液面上升,则说明气密性良好.
③注水法:用弹簧夹夹紧橡胶管,向长颈漏斗中加水,一段时间后,长颈漏斗内形成一段稳定的水柱,则装置气密性良好.
分析 根据装置气密性检查的原理一般是通过压强差来产生明显的现象来判断.压强差主要来自两方面:一是利用温度的变化引起气体体积变化,二是利用外力产生压强差进行分析.
解答 解:①检验装置气密性的方法:把装置连接好后,用双手捂住试管后试管内气体受热膨胀,压强增大,如果装置气密性良好时导管口就会有气泡冒出;
②如果装置气密性良好,当向外拉活塞时锥形瓶内压强减小,外界大气要通过长颈漏斗进入锥形瓶,所以长颈漏斗下端口处有气泡冒出,当缓慢推活塞时,锥形瓶内压强减大,把水压入长颈漏斗中,若气密性好则会形成一段稳定的水柱;
③注水法:用弹簧夹夹紧橡胶管,向长颈漏斗中加水,一段时间后,长颈漏斗内形成一段稳定的水柱,则装置气密性良好.
故答案为:(1)把装置连接好后,用双手捂住试管;
导管口有气泡冒出;
②玻璃管口有气泡冒出,玻璃管内液面上升;
③长颈漏斗内形成一段稳定的水柱.
点评 装置气密性的好坏会直接影响实验的现象结果,所以在实验前一定要检查装置的气密性.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
3.将含有杂质的金属样品加入到70g7%的稀硫酸中,恰好完全反应(杂质不跟稀硫酸反应),在反应后得到的硫酸盐中,金属元素的质量分数为20%,则在该金属样品中,和稀硫酸反应的金属单质的质量是( )
| A. | 1.5g | B. | 1.3g | C. | 2.0g | D. | 1.2g |
15.工业上常利石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3和超细CaCO3.
Ⅰ.制备KClO3的流程如图:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
(1)操作a的名称是过滤,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,该操作中玻璃棒的作用是引流.
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是氯酸钾在该温度下的溶解度小.
(3)洗涤KClO3晶体时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图已知NH4Cl溶液呈酸性.
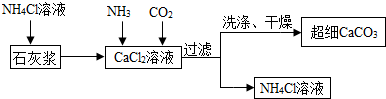
(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.该流程可循环使用的物质是NH4Cl.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加AB(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
Ⅰ.制备KClO3的流程如图:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是氯酸钾在该温度下的溶解度小.
(3)洗涤KClO3晶体时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图已知NH4Cl溶液呈酸性.

(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.该流程可循环使用的物质是NH4Cl.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加AB(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
12.下列实验现象描述不正确的是( )
| A. | 氢气在空气中燃烧,产生淡蓝色火焰,放出热量 | |
| B. | 木炭在氧气中燃烧,发出白光,产生能使澄清石灰水变浑浊的气体 | |
| C. | 铁丝在氧气中燃烧,火星四射,并有四氧化三铁固体生成 | |
| D. | 硫在氧气中燃烧,发出蓝紫色火焰,并生成有刺激性气味的气体 |
9.如表是氯化钾和硝酸钾在不同温度时的溶解度.
(1)两种物质受温度影响较大的是KNO3;
(2)40℃时,50g水中溶解20.0g氯化钾恰好达到饱和;
(3)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是加入硝酸钾等;
(4)60℃时,硝酸钾饱和溶液中溶有少量氯化钾,提纯硝酸钾的方法是降温结晶.
| 温度/℃ | 20 | 40 | 60 | 80 | |
| 溶解度/g | KCI | 34.0 | 40.0 | 45.5 | 51.1 |
| KNO3 | 31.6 | 63.9 | 110 | 169 | |
(2)40℃时,50g水中溶解20.0g氯化钾恰好达到饱和;
(3)使接近饱和的硝酸钾溶液变为饱和溶液的一种方法是加入硝酸钾等;
(4)60℃时,硝酸钾饱和溶液中溶有少量氯化钾,提纯硝酸钾的方法是降温结晶.
10.学习化学帮助我们形成更好的生活方式,下列说法不正确的是( )
| A. | 食用蔬菜和水果可以补充维生素C | |
| B. | CO(NH2)2属于复合肥 | |
| C. | 地沟油经过化学方法的处理形成航空燃油,实现了变废为宝 | |
| D. | 用灼烧的方法区别棉花和羊毛 |
 NO和NO2具有下列不同性质,通常情况下,NO是无色气体,难溶于水;NO2是红棕色气体,易溶干水.如图,将一支充满NO2的试管倒立在盛水的烧杯中.NO2与水反应生成硝酸和一氧化氮,写出反应方程式3NO2+H2O=2HNO3+NO,反应完全后可能出现的实验现象有紫色石蕊变红、试管内气体颜色逐渐变浅(最终成无色)、试管内上升一段液柱.
NO和NO2具有下列不同性质,通常情况下,NO是无色气体,难溶于水;NO2是红棕色气体,易溶干水.如图,将一支充满NO2的试管倒立在盛水的烧杯中.NO2与水反应生成硝酸和一氧化氮,写出反应方程式3NO2+H2O=2HNO3+NO,反应完全后可能出现的实验现象有紫色石蕊变红、试管内气体颜色逐渐变浅(最终成无色)、试管内上升一段液柱.