题目内容
5.硬水中含有较多的可溶性的钙、镁的化合物.其中钙的化合物Ca(HCO3)2受热易分解,对其加热生成水和大量的气体,还有一种难溶性的固体,它是一种盐,该盐是水垢的成分之一.(1)提出问题:探究Ca(HCO3)2受热分解的另外两种生成物.
(2)猜想:①小鸿认为生成物中的气体可能是二氧化碳;②你认为生成物中的固体可能是碳酸钙;
(3)设计实验方案:请你设计出简单的实验来验证上述两种猜想(用化学方程式表示)
猜想①的证明将生成的气体通入澄清石灰水
猜想②的证明往固体中加入稀盐酸,并将生成的气体通入澄清石灰水.
分析 根据题目给出的信息:碳酸氢钙[Ca(HCO3)2]受热易分解,生成水和大量的气体,还有一种难溶性的化合物,它是水垢的成分之一.根据质量守恒定律确定该固体是含钙的化合物,又因为该固体是难溶物,所以可能为碳酸钙.生成的气体可能是二氧化碳,可以用澄清的石灰水来检验;碳酸钙可以用稀盐酸和澄清石灰水检验,据此分析解决此题即可.
解答 解:碳酸氢钙[Ca(HCO3)2]受热易分解,生成水和大量的气体,还有一种难溶性的化合物,它是水垢的成分之一.根据质量守恒定律确定该固体是含钙的化合物,又因为该固体是难溶物,所以可能为碳酸钙.
如果小鸿猜想正确:因二氧化碳与石灰水反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O,有沉淀生成,故石灰水变浑浊,即可判断该气体是CO2,据此设计验证即可.
如果你的猜想正确,因碳酸钙与盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,二氧化碳与石灰水反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O,有沉淀生成,故有气体生成,石灰水变浑浊,由此可判断该固体为CaCO3,据此设计实验即可.
故答案为:碳酸钙;将生成的气体通入澄清石灰水;往固体中加入稀盐酸,并将生成的气体通入澄清石灰水.
点评 本考点属于实验探究题,既有实验过程的探究,又有结论的探究.本题综合性比较强,但难度不大,属基础性实验探究题.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
15.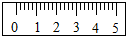 用托盘天平称量一未知质量的烧杯.现用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减少砝码.请用“↓”和“↑”在下表中表示你的称量过程,并在图中用“■”表示游码在标尺上的位置(若烧杯的实际质量为36.8g).
用托盘天平称量一未知质量的烧杯.现用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减少砝码.请用“↓”和“↑”在下表中表示你的称量过程,并在图中用“■”表示游码在标尺上的位置(若烧杯的实际质量为36.8g).
 用托盘天平称量一未知质量的烧杯.现用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减少砝码.请用“↓”和“↑”在下表中表示你的称量过程,并在图中用“■”表示游码在标尺上的位置(若烧杯的实际质量为36.8g).
用托盘天平称量一未知质量的烧杯.现用“↓”表示向托盘上增加砝码,用“↑”表示从托盘上减少砝码.请用“↓”和“↑”在下表中表示你的称量过程,并在图中用“■”表示游码在标尺上的位置(若烧杯的实际质量为36.8g).| 砝码(g) | 50 | 20 | 20 | 10 | 5 |
| 取用情况 |
10.下列不属于模型的是( )
| A. |  | B. |  足球烯 | ||
| C. |  | D. |  |
17.下列叙述正确的是( )
| A. | 纯净物一定是由分子构成的 | |
| B. | 由同种分子构成的物质一定是纯净物 | |
| C. | 混合物一定由两种或两种以上元素组成 | |
| D. | 只含有氧元素的物质一定是纯净物 |
14. 在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )
在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )
 在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )
在新能源汽车未普及时,如图所示为一种“节能减排”的有效措施.以下对乙醇作汽车燃料的描述错误的是( )| A. | 原料来源丰富 | |
| B. | 是可再生能源 | |
| C. | 燃烧完全没有污染 | |
| D. | 乙醇是以高粱、玉米等为原料制得的 |
15.雯雯在自学碳酸钠性质时,查到了以下资料:
①CO2+Na2CO3+H2O═2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液.
②碳酸钠、碳酸氢钠在不同温度下的溶解度
【进行实验1】验证CO2通入饱和碳酸钠溶液会产生白色沉淀
①配制碳酸钠溶液:取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液.
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2.
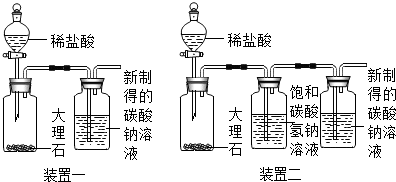
【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究.
【进行实验2】
(1)在0℃~30℃,Na2CO3和NaHCO3的溶解度受温度变化影响较大的是碳酸钠.
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
【进行实验3】
(4)雯雯在最初的实验中没有看到沉淀现象的原因是配制的碳酸钠溶液没有达到饱和.
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案.
①CO2+Na2CO3+H2O═2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液.
②碳酸钠、碳酸氢钠在不同温度下的溶解度
| 0℃ | 10℃ | 20℃ | 30℃ | |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
①配制碳酸钠溶液:取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液.
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2.

【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究.
【进行实验2】
| 实验操作 | 实验现象 |
| ①取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液 ②利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2 | 没有出现白色沉淀 |
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
【进行实验3】
| 实验操作 | 实验现象 |
| ①取100g热开水,加入35g碳酸钠固体,完全溶解,再降温至20℃,取上层清液 ②利用装置一和装置二分别进行实验,连续3分钟向新制得的碳酸钠溶液中通入CO2 | 装置一和装置二中的碳酸钠溶液中均出现白色沉淀 |
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案.
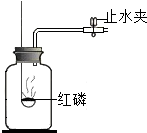 小聪和小明对竹子中气体的成分进行探究.他们把竹子浸泡在水中.在竹子上钻了一个小孔,看到有气泡从小孔中冒出.就收集了两瓶气体,第一瓶:采用如图所示的方法点燃红磷,有白烟生成.把装置放在水中,打开止水夹,进入集气瓶的水约占集气瓶体积的$\frac{1}{10}$.
小聪和小明对竹子中气体的成分进行探究.他们把竹子浸泡在水中.在竹子上钻了一个小孔,看到有气泡从小孔中冒出.就收集了两瓶气体,第一瓶:采用如图所示的方法点燃红磷,有白烟生成.把装置放在水中,打开止水夹,进入集气瓶的水约占集气瓶体积的$\frac{1}{10}$.