题目内容
3.小刚同学在做一定溶质质量分数的氯化钠溶液的配制实验时,其配制过程如图所示.试回答下列问题:
(1)写出图中有标号仪器的名称:a广口瓶,b烧杯.
(2)图示实验中有一处明显的错误是瓶塞没有倒放.图示实验中玻璃棒的作用是搅拌,加快溶解速率.
(3)在量取水的体积时,小刚同学俯视读数,所配制溶液中氯化钠的质量分数偏大(填“偏大”、“偏小”或“不变”).
分析 (1)根据常见的化学仪器的名称,进行分析解答.
(2)根据固体药品的取用方法、溶解操作中玻璃棒的作用,进行分析判断.
(3)在量取水的体积时,小刚同学俯视读数,读数比实际液体体积大,进行分析解答.
解答 解:(1)仪器a是广口瓶;仪器b是烧杯.
(2)取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,图中瓶塞没有倒放.
图示实验中玻璃棒的作用是搅拌,加快溶解速率.
(3)在量取水的体积时,小刚同学俯视读数,读数比实际液体体积大,会造成实际量取的水的体积偏小,则使溶质质量分数偏大.
故答案为:(1)广口瓶;烧杯;(2)瓶塞没有倒放;搅拌,加快溶解速率;(3)偏大.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
8.对比归纳是学习化学的重要方法.请你参与下列探究活动并回答问题:
实验一:探究影响硫燃烧剧烈程度的因素.
实验二:探究二氧化碳能否与氢氧化钠反应.
实验一:探究影响硫燃烧剧烈程度的因素.
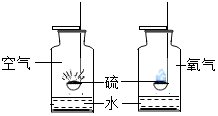 | 如左图,分别将硫在空气和氧气中燃烧. ①硫在氧气里燃烧比在空气里燃烧更剧烈,说明了影响硫燃烧剧烈程度的因素是氧气的浓度. |
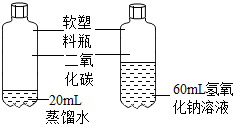 | 左图是小鹏同学设计的对比实验,用于证明二氧化碳和氢氧化钠能否反应.小燕同学认为该实验设计不符合对比实验的基本原则,她的理由是变量不唯一(或水和氢氧化钠溶液的体积不相等). |
 豆腐是生活中常见的食品,主要成分如图所示.
豆腐是生活中常见的食品,主要成分如图所示.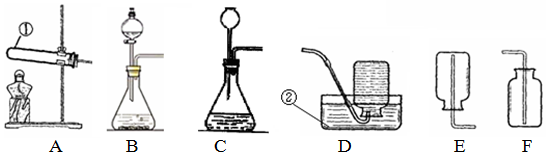

 量液时,量筒必须放平,视线要与量筒内液体凹液面的最低处保持水平再读出读数.如图表示的是某同学用50mL量筒最取一定体积液体的操作.请你仔细观察该图,判断量筒内液体的体积实际是小于(填大于、等于或小于)25mL.
量液时,量筒必须放平,视线要与量筒内液体凹液面的最低处保持水平再读出读数.如图表示的是某同学用50mL量筒最取一定体积液体的操作.请你仔细观察该图,判断量筒内液体的体积实际是小于(填大于、等于或小于)25mL.