题目内容
15.某学生称取一定量的高锰酸钾制氧气,待完全反应完毕后,制得氧气0.32g,则该学生称量的高锰酸钾的质量是多少克?(K:39 Mn:55 O:16)分析 高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,根据氧气的质量可以计算高锰酸钾的质量.
解答 解:设高锰酸钾的质量为x,
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
316 32
x 0.32g
$\frac{316}{x}$=$\frac{32}{0.32g}$,
x=3.16g,
答:该学生称量的高锰酸钾的质量是3.16g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
1. 如图是“小狗烯”(化学式为C26H26)的结构简式,下列说法正确的是( )
如图是“小狗烯”(化学式为C26H26)的结构简式,下列说法正确的是( )
 如图是“小狗烯”(化学式为C26H26)的结构简式,下列说法正确的是( )
如图是“小狗烯”(化学式为C26H26)的结构简式,下列说法正确的是( )| A. | 从类别上看:“小狗烯”属于有机物 | |
| B. | 从变化上看:“小狗烯”完全燃烧只生成水 | |
| C. | 从宏观上看:“小狗烯”由碳、氢二种原子组成 | |
| D. | 从微观上看:“小狗烯”由碳、氢二种元素构成 |
6.为了探究燃烧的条件,某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究.探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问.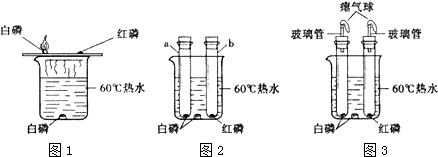
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
【变流与讨论】白烟对人体健康有害,该实验装置必须改进.
【改进与实验】同学们按改进后的图2装置进行实验.
请你帮助他们将下表补充完整.
【反思与评价】
(1)改进后的图2装置与图1装置比较,优点是防止白磷燃烧生成的五氧化二磷逸散到空气中,造成污染.
(2)王泽同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是:缓冲作用,防止胶塞冲出.
【拓展与迁移】
实验小结时,李颖同学说:“待a试管冷却恢复原温度后,如果将试管倒置水中,并在水中取下橡皮塞,将看到试管中液面升高.”这一说法得到大家的一致认同.
韩晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测:甲:接近试管容积的$\frac{1}{5}$;乙:小于试管容积的$\frac{1}{5}$.
你赞同的预测是甲 (填“甲”或“乙”),理由是:空气中氧气的体积约占空气体积的$\frac{1}{5}$,且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的$\frac{1}{5}$..

【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,…燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,可能与空气中水蒸气反应,生成有毒的偏磷酸(HPO3).
【变流与讨论】白烟对人体健康有害,该实验装置必须改进.
【改进与实验】同学们按改进后的图2装置进行实验.
请你帮助他们将下表补充完整.
| 现 象 | 解 释 |
| a试管中白磷燃烧,热水中白磷没有燃烧. b试管中红磷没有燃烧. | ①a试管中白磷燃烧的化学方程式是:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5; ②热水中白磷没有燃烧的原因是:达到着火点但没有和氧气接触; ③b试管中红磷没有燃烧的原因是:和氧气接触但没有达到着火点 |
(1)改进后的图2装置与图1装置比较,优点是防止白磷燃烧生成的五氧化二磷逸散到空气中,造成污染.
(2)王泽同学指出图2装置仍有不足之处,并设计了图3装置,其中气球的作用是:缓冲作用,防止胶塞冲出.
【拓展与迁移】
实验小结时,李颖同学说:“待a试管冷却恢复原温度后,如果将试管倒置水中,并在水中取下橡皮塞,将看到试管中液面升高.”这一说法得到大家的一致认同.
韩晶问:“如果不考虑橡皮塞占试管的容积,进入a试管内液体的体积会是多少呢?大家争论后,出现两种预测:甲:接近试管容积的$\frac{1}{5}$;乙:小于试管容积的$\frac{1}{5}$.
你赞同的预测是甲 (填“甲”或“乙”),理由是:空气中氧气的体积约占空气体积的$\frac{1}{5}$,且上述实验白磷足量、气密性良好,所以进入a试管内液体的体积能接近试管容积的$\frac{1}{5}$..
20.实验室里制取氢气和二氧化碳时,都可以选用的酸是( )
| A. | 稀HNO3 | B. | 稀HCl | C. | 稀H2SO4 | D. | 浓H2SO4 |
7.不法分子常用金光闪闪的“假金元宝”(铜锌合金)蒙骗人们,下列鉴别办法错误的是( )
| A. | 加盐酸 | B. | 测密度 | ||
| C. | 加硝酸银溶液 | D. | 看颜色 | ||
| E. | 在空气中充分灼烧 |
4.已知20℃时,食盐的溶解度是36克/100克水,则20℃时,5克饱和食盐水的溶质质量分数是( )
| A. | 18% | B. | 36% | C. | 26.5% | D. | 无法确定 |
5.质量守恒定律对科学发展具有重大意义.
(1)用如下图所示的3个实验装置进行实验,请写出A中发生的化学反应方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5,若要验证质量守恒定律,下列3个实验不能达到实验目的是B(填序号).

(2)由质量守恒定律可知,化学反应前后一定不变的是①②⑤(填序号).
①原子种类②原子数目③分子种类
④分子数目⑤元素种类⑥物质种类
(3)下列物质在密闭窗口内反应一段时间,测得反应前后各物质的质量如下:
①a的值为17.②该反应的基本反应类型是分解反应.
③Z一定是化合物(填“一定”或“不一定”).
(1)用如下图所示的3个实验装置进行实验,请写出A中发生的化学反应方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5,若要验证质量守恒定律,下列3个实验不能达到实验目的是B(填序号).

(2)由质量守恒定律可知,化学反应前后一定不变的是①②⑤(填序号).
①原子种类②原子数目③分子种类
④分子数目⑤元素种类⑥物质种类
(3)下列物质在密闭窗口内反应一段时间,测得反应前后各物质的质量如下:
| 物质 | X | Y | Z | W |
| 反应前质量/g | 12 | 2.2 | 16.2 | 0.9 |
| 反应后质量/g | a | 4.4 | 8.1 | 1.8 |
③Z一定是化合物(填“一定”或“不一定”).