题目内容
8.现有溶质质量分数为25%的氢氧化钠溶液300克.(1)这300克氢氧化钠溶液中含有氢氧化钠75克,水225克.
(2)若将此溶液稀释成10%的氢氧化钠溶液需加水多少毫升?
分析 利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量;再根据溶剂质量=溶液质量-溶质质量即可求得水的质量.在溶液稀释过程中,溶质的质量不变列等式.
解答 解:(1)配制300g溶质质量分数为25%的氢氧化钠溶液,需要氢氧化钠的质量为300g×25%=75g;溶剂质量=溶液质量-溶质质量,则所需水的质量=300g-75g=225g.
(2)可根据稀释前后溶质的质量守恒求解.
设需加入水的质量为x.
300g×25%=(300g+x)×10%
解之得 x=450g
需要水的体积为$\frac{450g}{1g/mL}$=450mL
答:(1)需要氢氧化钠的质量和水的质量分别为75g、225g.
(2)需加水450mL.
点评 本题难度不大,掌握溶质质量=溶液质量×溶质的质量分数、溶剂质量=溶液质量-溶质质量和溶液稀释过程中溶质质量不变是正确解答本题的关键.

练习册系列答案
相关题目
19.化学课后,化学兴趣小组的同学在整理实验桌时,发现有一瓶氢氧化钠溶液没有塞橡皮塞,征得老师同意后,开展了以下探究:
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
【提出问题2】该氢氧化钠溶液是全部变质还是部分变质呢?
【猜想与假设】猜想1:氢氧化钠溶液部分变质;猜想2:氢氧化钠溶液全部变质.
【查阅资料】①氯化钙溶液呈中性;②氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl.
【实验探究2】
【实验结论】该氢氧化钠溶液部分(填“部分”或“全部”)变质.
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(2)在上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:澄清石灰水.
【提出问题1】该氢氧化钠溶液是否变质了呢?
【实验探究1】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量该溶液与试管中,向溶液中滴加盐酸,并不断振荡 | 有气泡冒出 | 氢氧化钠溶液一定变质了 |
【猜想与假设】猜想1:氢氧化钠溶液部分变质;猜想2:氢氧化钠溶液全部变质.
【查阅资料】①氯化钙溶液呈中性;②氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3=CaCO3↓+2NaCl.
【实验探究2】
| 实验步骤 | 实现现象 | 实验结论 |
| (1)取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,并不断振荡 | 有 白色沉淀生成 | 说明溶液中一定由碳酸钠 |
| (2)取步骤(1)试管中的少量上层清液,滴加酚酞试液 | 溶液变成红色 | 说明原溶液中一定有 氢氧化钠 |
【反思与评价】
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式:CO2+2NaOH=Na2CO3+H2O.
(2)在上述【实验探究2】中,小明提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案不可行(填“可行”或“不可行”).
【理解与应用】氢氧化钠溶液容易变质,必须密封保存.实验室必须密封保存的药品还有很多,试另举一例:澄清石灰水.
16.生物体内几乎所有的化学反应均在酶的参与下才能完成,以下有关酶的说法不正确的是( )
| A. | 酶只能在细胞内起作用 | |
| B. | 一种酶只能催化某一种或某一类化学反应 | |
| C. | 酶的催化作用受到温度、pH 的影响 | |
| D. | 酶是生物体细胞制造的一种蛋白质 |
20. 小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:
小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:
(1)猜想:瓶口的白色固体可能是碳酸钠.基于这样猜想的理由是:因为空气中含有空气中含有二氧化碳,氢氧化钠能与二氧化碳反应生成碳酸钠;
实验:他们取下一小块白色固体于试管中并加入稀盐酸,看到固体迅速溶解并产生大量气泡,从而证实了小柯的假设.
(2)请你帮他们完成验证该试剂是否已全部变质的设计方案:
(3)一定质量的NaOH溶液,变质前和变质后与盐酸反应时,所用盐酸的质量是否相同,判断并说明理由相同,因为一定质量的氢氧化钠变质程度不同,所含钠元素质量相同,相同质量的钠元素生成氯化钠时消耗氯化氢的质量相同.
 小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:
小胖做化学实验时,在橱柜里发现NaOH的瓶中有大量白色固体(如图).为了知道固体是什么物质,展开了探究:(1)猜想:瓶口的白色固体可能是碳酸钠.基于这样猜想的理由是:因为空气中含有空气中含有二氧化碳,氢氧化钠能与二氧化碳反应生成碳酸钠;
实验:他们取下一小块白色固体于试管中并加入稀盐酸,看到固体迅速溶解并产生大量气泡,从而证实了小柯的假设.
(2)请你帮他们完成验证该试剂是否已全部变质的设计方案:
| 探究步骤 | 现象 | 结论 |
| ①取少量试剂于试管,向其中滴加足量的氯化钙溶液 | 产生白色沉淀 | 试剂中含有碳酸钠 |
| ②在①完全反应所得的清液中,滴加酚酞溶液 | 酚酞溶液变红 | 试剂中含有氢氧化钠 |

 (1)如图为电解水实验的装置图,CD试管之间产生气体的体积比约为2:1.
(1)如图为电解水实验的装置图,CD试管之间产生气体的体积比约为2:1. 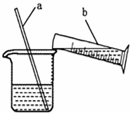 图是稀释浓硫酸实验的示意图.
图是稀释浓硫酸实验的示意图. 某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验.