题目内容
18.在实验室常采用固体氯化铵(NH4Cl)和熟石灰[Ca(OH)2]共热来制取氨气(NH3),已知氨气属于碱性气体,会和酸反应生成铵盐,密度比空气小,且极易溶于水.制取氨气时反应的化学方程式为:2NH4Cl(固)+Ca(OH)2(固)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O据此回答:

(1)制取氨气时某同学从如图中选择了反应的发生装置和收集装置,你认为正确的组合应该是B.
A.A和C B.A和D C.B和E D.B和D
(2)某同学为了获得干燥的氨气,于是想在发生装置和收集装置之间加装一个干燥装置,那么你觉得该干燥装置中的物质可否用浓硫酸?试写出理由(可用化学方程式):2NH3+H2SO4=(NH4)2SO4.
分析 制取装置包括加热和不需加热两种,在实验室常采用固体氯化铵(NH4Cl)和熟石灰[Ca(OH)2]共热来制取氨气(NH3),因此需要加热;已知氨气属于碱性气体,会和酸反应生成铵盐,密度比空气小,且极易溶于水,因此只能用向下排空气法收集.题目的信息中没有反映出氨气的用途;氨气不能用浓硫酸干燥,氨气和硫酸反应生成硫酸铵,配平即可
解答 解:(1)在实验室常采用固体氯化铵(NH4Cl)和熟石灰[Ca(OH)2]共热来制取氨气(NH3),因此需要加热;已知氨气属于碱性气体,会和酸反应生成铵盐,密度比空气小,且极易溶于水,因此只能用向下排空气法收集;故答案为:B;
(2)氨气不能用浓硫酸干燥,氨气和硫酸反应生成硫酸铵,配平即可;故答案为:不能;2NH3+H2SO4=(NH4)2SO4;
故答案为:
(1)B;
(2)H2SO4+2NH3=(NH4)2SO4.
点评 本考点主要考查了气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
8.为测定其真实的含钙量,孙东同学每次取10片钙片放入已称量的含足量盐酸的烧杯中,钙片中除CaCO3 外,其它成分不与HCl反应.充分反应后再称取烧杯和剩余物的总质量.孙东同学做了三次实验,数据如表:
请列式计算每片这样的钙片含碳酸钙的质量.
| 物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
| 反应前;烧杯+盐酸 | 22g | 22g | 22g | 22g |
| 10片钙片 | 8g | 8g | 8g | 8g |
| 反应后;烧杯+剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
9.下列图象不能正确反映对应变化关系的是( )
| A. | 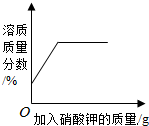 20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体 | |
| B. | 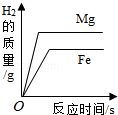 将等质量的镁片和铁片投入到足量稀硫酸中 | |
| C. | 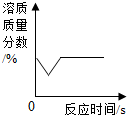 向某温度下一定量的熟石灰饱和溶液中加入少量生石灰 | |
| D. | 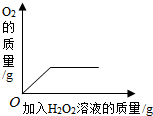 向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液 |
6.如图甲是氢气和氧化铜反应的实验,如图乙是木炭和氧化铁反应的实验.
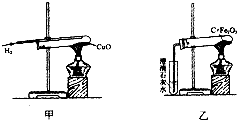
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中 也未产生预期的气泡,这说明该反应并没有生成铁.
(3)该同学查阅资料,得到关于铁的氧化物如下信息:
根据以上信息,试写出乙实验试管中反应的化学方程式C+6Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$4Fe3O4+CO2↑.
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.

(1)在上述两个实验中,氢气和木炭表现出相同的化学性质是还原性.
(2)某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中 也未产生预期的气泡,这说明该反应并没有生成铁.
(3)该同学查阅资料,得到关于铁的氧化物如下信息:
| 铁的氧化物化学式 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红 | 黑 | 黑 |
| 化学性质 | 可溶于酸 | 常温下不溶于稀酸 | 可溶于酸 |
经分析后,该同学试着提高反应温度后,实验出现了预期的现象.
13.下列有关化学反应A+B=C+D的叙述中,正确的是( )
| A. | 若C和D分别是盐和水,那么A和B一定是酸和碱 | |
| B. | 若B和D是单质,A和C是化合物,该反应一定是置换反应 | |
| C. | 若A、B各取5克充分反应,则C、D质量总和一定等于10克 | |
| D. | A和B的质量比一定等于C和D的质量比 |
3.下面是李好同学用连线的方式对某一主题知识进行归纳的情况,其中有错误的一组是( )
| A. | 性质与用途 氢气燃烧产物为水--最理想燃料熟石灰呈碱性--改良酸性土壤 悬挂起来分别羊毛线与棉线一一灼烧 | |
| B. | 元素与人体健康 人体缺氟--易生龋牙缺钙元素--得佝偻病人体缺碘--甲状腺肿大 | |
| C. | 生活常识 减少水污染--合理使用农药、化肥减少汽车尾气污染--使用乙醇汽油减少白色污染--使用可降解的塑料食品 | |
| D. | 环保与物质的利用 活性炭有吸附性--做净水剂 干燥剂--常用生石灰防菜刀生锈--喷水后 |
7.下列化学方程式书写正确合理的是( )
| A. | Cu+H2SO4═CuSO4+H2↑ | B. | Fe+6HCl═2FeCl3+3H2↑ | ||
| C. | 2Al+6HCl═2AlCl3+3H2↑ | D. | CaCl2+2KNO3═Ca(NO3)2+2KCl |