题目内容
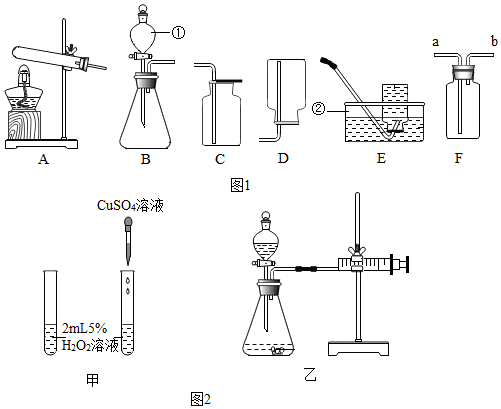
7.实验室图1现有氯酸钾、二氧化锰、过氧化氢溶液、硫酸铜溶液、稀盐酸、稀硫酸、大理石,以及制取气体的常用装置:(1)标号仪器②的名称:水槽;
(2)上述装置中的A和E组合后,可以用来制取并收集的气体是氧气,写出实验室制取该气体的化学方程式:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,F装置也可用于收集该气体,该气体应从a(填“a”或“b”)进入F中.
(3)实验室制取二氧化碳的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑,标号仪器①可用于控制反应的速率.
(4)过氧化氢溶液在常温下能缓慢的产生氧气,硫酸铜溶液对过氧化氢的分解有催化作用.某同学设计了图2甲图对其催化效果进行了探究:
①如图2甲,实验室观察并对比两支试管中的现象,根据产生气泡的快慢判断硫酸铜溶液对过氧化氢分解反应快慢的影响,该反应的化学方程式为2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑.
②图2乙不仅可用于制备氧气,还可测量氧气的体积,实验前,老师按照如图所示装置连接后,向右拉动活塞,然后松手,看活塞能否回到原处,老师这么做的目的是检查装置的气密性.
分析 水槽是盛水的仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.图2乙不仅可用于制备氧气,还可测量氧气的体积;实验前,老师按照如图所示装置连接后,向右拉动活塞,然后松手,看活塞能否回到原处,是为了检查装置的气密性.
解答 解:(1)水槽是盛水的仪器,故答案为:水槽;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;F装置也可用于收集该气体,该气体应从长管进入,因为氧气的密度比空气的密度大,故答案为:氧气;2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;a;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;分液漏斗可以控制反应的速率;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;控制反应的速率;
(4)如图2甲,实验室观察并对比两支试管中的现象,根据产生气泡的快慢,判断硫酸铜溶液对过氧化氢分解反应快慢的影响;图2乙不仅可用于制备氧气,还可测量氧气的体积;实验前,老师按照如图所示装置连接后,向右拉动活塞,然后松手,看活塞能否回到原处,是为了检查装置的气密性;故答案为:气泡的快慢;检查装置的气密性;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、检查装置的气密性等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | HCl(CO2) | 适量NaOH溶液 | 洗气 |
| B | NaCl(Na2CO3) | 适量稀硫酸 | 蒸发、结晶 |
| C | CaO(CaCO3) | 足量水 | 溶解、过滤、干燥 |
| D | FeCl2溶液(CuCl2) | 加入过量铁粉 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 有盐和水生成的反应不一定是中和反应 | |
| B. | 由同种元素组成的物质不一定是单质 | |
| C. | 同种元素的原子和离子的质子数不一定相同 | |
| D. | 同一化合物中同种元素的化合价不一定相同 |
| A. |  点燃酒精灯 | B. |  倾倒液体 | C. |  量取液体 | D. |  检查气密性 |
 A、B两图分别表示硫、铁丝在氧气中燃烧的示意图.请填空:
A、B两图分别表示硫、铁丝在氧气中燃烧的示意图.请填空:
